IA en Cardiología Nuclear: ¿Qué está cambiando?

¿Qué pasaría si pudiéramos ver no solo la estructura del corazón, sino cuán bien funciona realmente? Eso es exactamente lo que la cardiología nuclear hace posible.
La cardiología nuclear utiliza trazadores radiactivos para evaluar la función cardíaca, el flujo sanguíneo y la viabilidad del tejido. Permite un diagnóstico temprano y no invasivo de condiciones como la enfermedad de las arterias coronarias y la amiloidosis cardíaca, ofreciendo un cuidado cardíaco más preciso y personalizado.
Descubre cómo tecnologías como PET, SPECT, IA y nuevos radiotrazadores están transformando el futuro de los diagnósticos cardíacos

¿Qué es la cardiología nuclear?
La cardiología nuclear es una subespecialidad de la imagen cardiovascular que revela cómo funciona el corazón. Utiliza pequeñas cantidades de sustancias radiactivas (radiotrazadores) para rastrear el flujo sanguíneo, medir la actividad del músculo cardíaco y evaluar la salud cardíaca desde el interior.
A diferencia de las tomografías computarizadas o resonancias magnéticas, que muestran la estructura física del corazón, la cardiología nuclear se enfoca en el metabolismo, la perfusión y la función.Esto significa que puede detectar si una parte del corazón está recibiendo suficiente sangre y si todavía es viable, mucho antes de que aparezca un daño estructural en una exploración estándar.
Este enfoque se ha vuelto esencial en el diagnóstico de condiciones cardíacas complejas o en etapa temprana. Por ejemplo, una arteria coronaria puede parecer estrechada en un angiograma.
¿Sin embargo, realmente esa obstrucción está restringiendo el flujo sanguíneo?
La cardiología nuclear responde esa pregunta con claridad.
También permite pruebas más seguras y no invasivas en pacientes que de otro modo necesitarían procedimientos más invasivos, como biopsias o cateterismos.
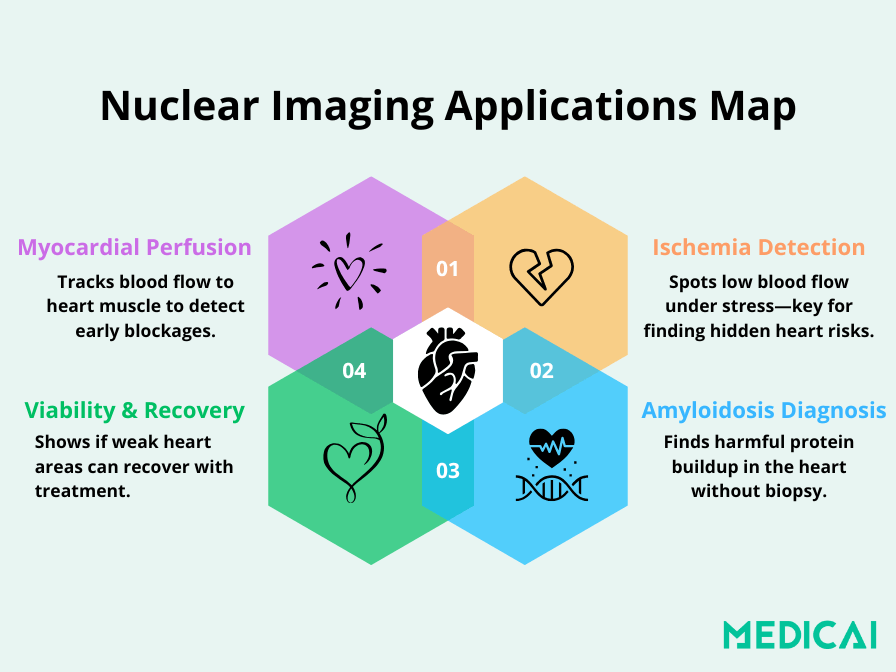
Aplicaciones principales de la cardiología nuclear en la práctica clínica
La cardiología nuclear se utiliza ampliamente para:
- Evaluar la perfusión miocárdica (flujo sanguíneo al músculo cardíaco)
- Diagnosticar o monitorear la enfermedad de las arterias coronarias (EAC)
- Evaluar el daño después de un ataque al corazón
- Determinar si los pacientes necesitan stents o cirugía de bypass
- Monitorear los efectos de tratamientos cardiotóxicos (como la quimioterapia)
- Detectar enfermedades raras como la amiloidosis cardíaca sin necesidad de biopsia
La cardiología nuclear permite a los clínicos detectar problemas cardíacos antes de que los síntomas se vuelvan graves o notorios. Por eso es clave en la detección de pacientes de alto riesgo, seguimiento de la recuperación postquirúrgica y optimización de estrategias de tratamiento a largo plazo.
En esencia, la cardiología nuclear cambia el foco de cómo se ve el corazón a cómo funciona, y ese cambio salva vidas.
De la Biopsia al Avance: Imagenología Nuclear en el Diagnóstico Cardíaco
Ciertas condiciones cardíacas, particularmente la amiloidosis cardíaca, solían diagnosticarse mediante un procedimiento llamado biopsia endomiocárdica. Aunque efectivo, es invasivo, requiere la inserción de un catéter en el corazón y conlleva riesgos como sangrado, infección o incluso perforación.
También exige entrenamiento experto y centros altamente especializados.
Hoy, la cardiología nuclear está cambiando eso. Usando radiotrazadores dirigidos, los clínicos pueden detectar depósitos de amiloide en el corazón de forma no invasiva, a menudo con igual o mayor precisión, y mucho antes de que los síntomas se vuelvan severos.
Uno de los cambios más impactantes es el diagnóstico de la amiloidosis cardíaca, una condición en la que las proteínas mal plegadas se acumulan en el corazón, haciéndolo rígido y menos eficiente. Hay dos tipos principales:
- Amiloidosis ATTR, vinculada a la proteína transtiretina y a menudo relacionada con la edad
- Amiloidosis AL, que involucra cadenas ligeras de células plasmáticas
Estos subtipos requieren tratamientos completamente diferentes, lo que hace que la diferenciación temprana y precisa sea crucial. La imagenología nuclear lo hace posible.
En lugar de muestreo de tejido, los clínicos utilizan trazadores que buscan hueso como 99mTc-PYP o 99mTc-DPD para diagnosticar ATTR con alta confianza. Cuando es necesario descartar la amiloidosis AL, se añaden pruebas de laboratorio para proteínas séricas y urinarias.
Para casos más complejos, trazadores PET como 11C-PiB o 18F-florbetaben ofrecen incluso mayor especificidad, particularmente en la detección del involucramiento AL y el monitoreo de la respuesta al tratamiento.
Lo que solía ser una biopsia hospitalaria compleja ahora puede ser reemplazado por una exploración y algunas pruebas de sangre. Este avance está mejorando los tiempos de diagnóstico, el confort del paciente y el acceso a la atención.
Más estudios muestran que las herramientas de imagen diagnostican y predicen el pronóstico y rastrean la efectividad del tratamiento, permitiendo un cuidado cardíaco más personalizado.

Imagen de Perfusión Miocárdica (MPI): El Corazón de la Cardiología Nuclear
La imagen de perfusión miocárdica, o MPI, es una de las técnicas más establecidas y confiables en la cardiología nuclear. Es una exploración no invasiva que evalúa cuán bien fluye la sangre al músculo cardíaco.
MPI compara la perfusión en reposo y durante el estrés para ayudar a los clínicos a identificar áreas del corazón que pueden carecer de suficiente sangre rica en oxígeno antes de que los síntomas como el dolor en el pecho o la fatiga empeoren.
Este enfoque de doble fase es vital. Cuando una región del corazón muestra un flujo sanguíneo reducido bajo estrés pero se ve normal en reposo, típicamente señala isquemia reversible. Es una señal de advertencia de una posible enfermedad de las arterias coronarias (EAC) significativa.
Por otro lado, si un defecto está presente tanto en las exploraciones de estrés como en reposo, sugiere tejido cicatricial o daño miocárdico previo.
La Ciencia Detrás de la Exploración
Los radiotrazadores son centrales en el funcionamiento de MPI. Una vez inyectados en el torrente sanguíneo, estas sustancias imitan los patrones de flujo sanguíneo y se acumulan en el tejido cardíaco saludable. Las áreas que toman menos trazador aparecen como “puntos fríos” en la exploración, indicando pobre perfusión.
Los trazadores comunes usados para MPI incluyen:
- Compuestos de Tecnecio-99m, como sestamibi (MIBI) y tetrofosmina, son ampliamente usados en la imagen SPECT debido a la buena calidad de imagen y la vida media favorable
- El Talio-201, un trazador más antiguo con una vida media más larga, todavía se usa en casos selectos para la evaluación de la viabilidad
- Los trazadores PET como Rubidio-82, Amoníaco de Nitrógeno-13 y el recientemente aprobado F18-Flurpiridaz por la FDA ofrecen alta resolución para evaluar sospechas de EAC.
Cada trazador tiene sus fortalezas, pero todos tienen el mismo objetivo: mostrar cuán bien llega la sangre al corazón bajo diferentes condiciones.
¿Por qué MPI es Importante en la Práctica Clínica?
MPI es más que una herramienta de diagnóstico; a menudo es la primera exploración para identificar problemas de salud serios. Los clínicos dependen de MPI para:
- Detectar la enfermedad de las arterias coronarias (EAC), incluso antes de que cause síntomas notables
- Evaluar la severidad de la limitación del flujo sanguíneo, especialmente cuando el estrés físico o farmacológico revela isquemia oculta
- Evaluar el riesgo de futuros ataques cardíacos y muerte cardíaca
- Guiar las estrategias de tratamiento, como elegir entre medicación, angioplastia o cirugía de bypass
- Monitorear la recuperación después de un ataque al corazón o procedimiento quirúrgico
MPI tiene un valor pronóstico significativo, con resultados normales indicando un bajo riesgo anual de eventos cardíacos similar a la población general. Cuando se detectan anormalidades, el grado de flujo sanguíneo reducido ayuda en la estratificación del riesgo e influye en la planificación del tratamiento.
SPECT vs PET: Elegir la Modalidad Correcta
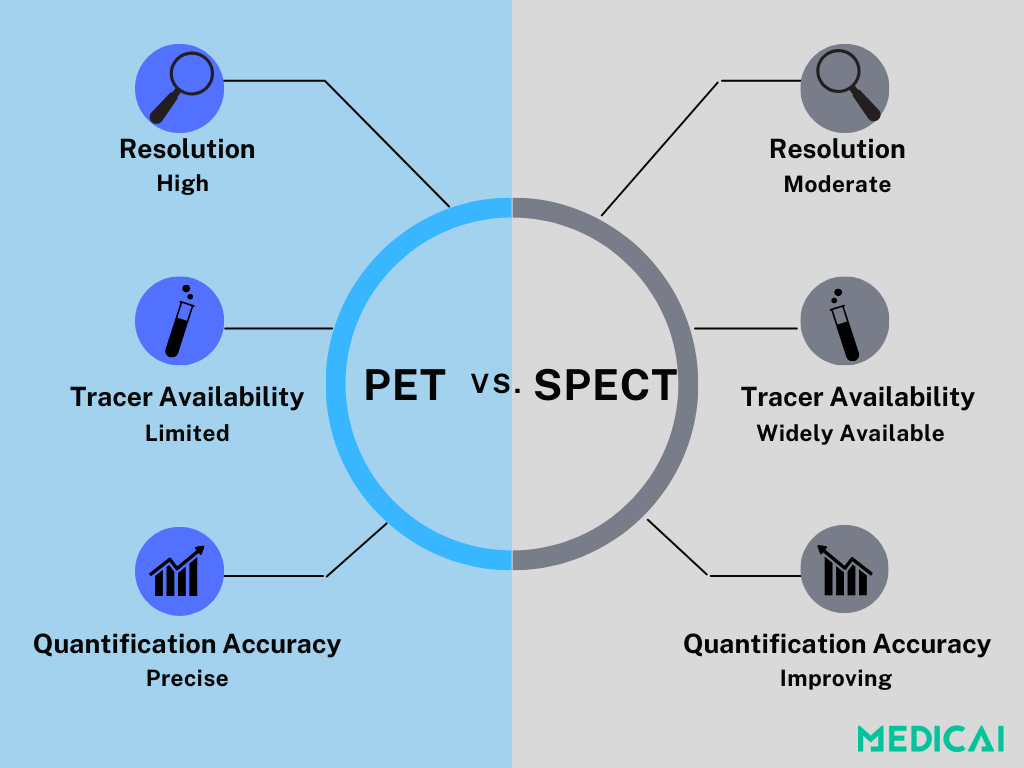
Mientras que tanto SPECT como PET se usan en la imagen de perfusión miocárdica (MPI), difieren en áreas clave: resolución, precisión de cuantificación, disponibilidad y costo.
PET es el estándar de oro para cuantificar el flujo sanguíneo miocárdico (MBF). Su mayor resolución espacial y la capacidad de medir el flujo sanguíneo en términos absolutos lo hacen especialmente útil para evaluar enfermedades coronarias complejas o sutiles.
Sin embargo, PET sigue siendo limitado por el costo y la accesibilidad. Trazadores especializados como Rubidio-82, N-13 amoníaco y F18-Flurpiridaz son caros y no están disponibles. Muchos escáneres PET también se priorizan para oncología, haciendo que el uso cardíaco sea menos viable en muchas regiones.
Por otro lado, SPECT es mucho más accesible y utiliza trazadores ampliamente disponibles como Tecnecio-99m MIBI y Tetrofosmina. Aunque no iguala la precisión de PET, las tecnologías más nuevas como los detectores CZT (Telurio de Cadmio Zinc) han mejorado significativamente la calidad de imagen, velocidad y sensibilidad.
Con el desarrollo ahora de SPECT dinámico y reconstrucción asistida por AI, SPECT está ganando terreno como una opción más práctica y económica para la evaluación de MBF, particularmente donde el acceso a PET es limitado.
A medida que las tecnologías SPECT y CZT avanzan, soluciones como Medicai pueden mejorar la calidad de imagen y estandarizar protocolos, ayudando a cerrar la brecha de rendimiento con PET.
Al final, elegir entre los dos es una cuestión de equilibrar el rendimiento con la practicidad. PET ofrece una cuantificación inigualable, pero SPECT está evolucionando rápidamente, y para muchas clínicas, es el camino más realista hacia adelante en la cardiología nuclear.
Amiloidosis Cardíaca: Cómo la Imagenología Nuclear Está Redefiniendo el Diagnóstico
La amiloidosis cardíaca se diagnosticaba tradicionalmente a través de biopsia, un procedimiento arriesgado y especializado. Ahora, la cardiología nuclear permite una detección y clasificación no invasivas y más tempranas de esta compleja condición.
La amiloidosis es causada por la acumulación de proteínas mal plegadas en el corazón, que interfieren con su capacidad para funcionar adecuadamente. Dos tipos principales afectan al corazón:
- ATTR (amiloidosis de transtiretina) – a menudo relacionada con la edad o hereditaria
- AL (amiloidosis de cadenas ligeras) está asociada con trastornos de las células plasmáticas
Estos dos tipos difieren en patología y tratamiento, por lo que distinguir entre ellos es crítico. La biopsia puede hacerlo, pero es invasiva. Ahora la imagenología nuclear ofrece una alternativa más segura.
El Auge de los Trazadores Ávidos del Hueso
El uso de trazadores que buscan hueso como 99mTc-PYP, 99mTc-DPD y 99mTc-HMDP ha mejorado dramáticamente el diagnóstico de amiloidosis ATTR. La fuerte captación de radiotrazadores en el corazón (Grado 2 o 3) combinada con pruebas de sangre regulares para proteínas monoclonales confirma el diagnóstico sin necesidad de biopsia.
Este enfoque mejora la accesibilidad y permite la detección más temprana de enfermedades, a menudo antes de que ocurra un daño irreversible al corazón.
Imagen PET: Un Nuevo Horizonte para la Amiloidosis AL
Mientras que los trazadores óseos son excelentes para ATTR, son menos confiables para la amiloidosis AL. Aquí es donde entra en juego la imagen PET.
Usando trazadores como 11C-PiB, 18F-florbetaben o 18F-florbetapir, PET puede unirse directamente a las proteínas amiloides y visualizar tanto los subtipos AL como ATTR, con una tendencia a mostrar incluso mayor captación en casos AL.
Los estudios muestran que PET ayuda a diferenciar los tipos de amiloide y proporciona conocimientos sobre la carga de la enfermedad y la respuesta al tratamiento. Para los pacientes con amiloidosis AL en quimioterapia, los cambios en la señal PET pueden indicar la efectividad de la terapia, revolucionando el monitoreo de la enfermedad.
Más allá de la Perfusión: El Kit de Herramientas en Expansión de la Cardiología Nuclear
La imagen de perfusión miocárdica (MPI) es central en la cardiología nuclear. Sin embargo, el campo se ha expandido para incluir técnicas que evalúan el metabolismo miocárdico, la actividad nerviosa y la viabilidad tisular, mejorando los diagnósticos cardíacos en el cuidado de la insuficiencia cardíaca.
FDG-PET es una de esas herramientas. La imagen de la captación de glucosa en el músculo cardíaco ayuda a detectar miocardio hibernante. Este tejido está vivo pero funciona mal debido a un flujo sanguíneo crónicamente bajo. El área puede recuperarse con revascularización si se toma glucosa a pesar de una contracción débil.
Esto hace que FDG-PET sea especialmente valiosa en pacientes con disfunción ventricular izquierda isquémica, guiando decisiones sobre cirugía de bypass u otras intervenciones.
Otra opción emergente es la imagen de yodo-123 mIBG, que evalúa la inervación simpática del corazón. La reducción de la captación mIBG en pacientes con insuficiencia cardíaca se ha vinculado a peores resultados, ofreciendo a los clínicos una herramienta adicional para la evaluación del riesgo y planificación del tratamiento.
Aunque no es ampliamente adoptadas, estas técnicas significan un cambio de observar meramente la estructura del corazón a entender su comportamiento metabólico, eléctrico y funcional. A medida que emerge más evidencia, están destinadas a mejorar el cuidado cardíaco personalizado.
IA y la Imagen Cuantitativa: El Próximo Gran Salto Adelante
A medida que la imagen nuclear evoluciona, la IA simplifica y mejora el proceso. Las exploraciones proporcionan datos detallados sobre el flujo sanguíneo, función y riesgo, haciendo que la gestión eficiente de datos sea crucial para una toma de decisiones más rápida.
La IA es particularmente útil en la cuantificación del flujo sanguíneo miocárdico (MBF), especialmente en la imagen PET. Automatiza la reconstrucción de imágenes, segmentación y análisis de flujo, reduciendo pasos manuales y la variabilidad entre los clínicos.
Las herramientas de IA están optimizando la reconstrucción de imágenes, segmentación y cuantificación del flujo sanguíneo. Plataformas como Medicai integran datos de múltiples modalidades en herramientas de soporte en tiempo real, reduciendo la variabilidad y mejorando la confianza diagnóstica.
La IA también respalda SPECT dinámico, donde se necesita una imagen rápida para estimar el MBF. Con mejores algoritmos y detectores como CZT, SPECT está acercándose a las capacidades a nivel PET.
Más allá de la cuantificación, la IA está entrenada para predecir resultados analizando patrones en la perfusión, función y captación extraconcarga. Estos modelos podrían ayudar pronto a los clínicos a estratificar el riesgo con mayor precisión.
La IA no está reemplazando a los radiólogos; está mejorando su trabajo, haciendo la imagenología más inteligente y rápida, y conduciendo a mejores diagnósticos cardíacos personalizados.
Conclusión
La cardiología nuclear está transformando el cuidado del corazón al priorizar la función sobre la anatomía, permitiendo diagnósticos más tempranos y precisos. Los avances clave incluyen la imagen de perfusión, la cuantificación impulsada por IA y la detección de amiloidosis a través de tecnologías como PET, CZT-SPECT y la imagen funcional.
Plataformas como Medicai ayudan a los clínicos a analizar datos cardíacos con mayor precisión y eficiencia. Al combinar la automatización con la visión clínica, permitimos diagnósticos cardíacos personalizados y escalables.
Artículos relacionados



¡Pongámonos en contacto!
Descubra cómo Medicai puede ayudarle a fortalecer su consulta y mejorar la experiencia de sus pacientes. ¿Listo para comenzar su viaje?
Reserve una demostración gratuita