Segmentación de Imágenes de Resonancia Magnética de Tumores Cerebrales Usando Técnicas de Aprendizaje Profundo
Imagina reducir horas de segmentación manual de MRI cerebral a segundos.
Los límites de los tumores cerebrales emergen automáticamente, y el aprendizaje profundo está haciendo esto posible. Aporta precisión, velocidad y consistencia a los flujos de trabajo en neuro-oncología.
El aprendizaje profundo aprovecha las CNN, U-Nets de atención y híbridos de transformadores para segmentar automáticamente exploraciones de MRI multimodal. Estos modelos superan a los métodos clásicos en términos de velocidad, precisión y reproducibilidad, permitiendo una delimitación precisa de los límites tumorales para su uso clínico en diversos entornos.
Descubre la segmentación de imágenes de MRI de tumores cerebrales utilizando técnicas de aprendizaje profundo: arquitecturas básicas, conjuntos de datos e impactos clínicos.

¿Qué es la segmentación de tumores cerebrales basada en MRI?
La segmentación de tumores cerebrales basada en MRI divide las exploraciones de MRI en regiones etiquetadas, separando el tejido tumoral de las estructuras cerebrales sanas. Cada voxel se agrupa por características compartidas, incluyendo-
- Intensidad
- Textura
- Límites
Crean un mapa claro de subregiones tumorales.
Este agrupamiento automatizado reemplaza la conjetura con etiquetas precisas y basadas en datos. La segmentación es el primer paso crítico para cualquier análisis posterior.
En la segmentación manual, los radiólogos expertos dibujan meticulosamente los contornos tumorales en cada sección de la imagen. Este trazado sección por sección puede llevar horas por caso y varía según el lector.
Los modelos automatizados de aprendizaje profundo aprenden a predecir estos contornos en segundos. Las herramientas semi-automáticas todavía necesitan alguna corrección del usuario; las redes completamente automáticas ofrecen predicciones de extremo a extremo sin entrada manual.
Una encuesta destaca que las redes profundas superan a los métodos clásicos tanto en velocidad como en consistencia.
La segmentación precisa impulsa una mejor atención.
- Proporciona mediciones de volumen precisas para la planificación de la terapia de radiación.
- Estandariza regiones para la extracción de características radiómicas, generando biomarcadores confiables.
- En el quirófano, mapas tumorales 3D claros guían a los cirujanos para maximizar la resección mientras preservan el tejido sano.
Así, la segmentación automatizada acelera los flujos de trabajo y respalda la neuro-oncología personalizada.
¿Por qué aprendizaje profundo para la segmentación de imágenes de MRI de tumores cerebrales?
Las técnicas de procesamiento de imágenes clásicas, como el umbral y el crecimiento de regiones, segmentan tumores agrupando píxeles con intensidades similares o proximidad espacial. Dificultan cuando los límites tumorales son difusos o cuando la intensidad se superpone con el tejido sano.
Estos métodos a menudo requieren ajustes manuales de umbrales para cada paciente y fallan en presencia de ruido en la MRI o configuraciones de escáner variables.
Las redes neuronales convolucionales (CNN) superan estos límites al aprender jerarquías de características directamente de los datos. Las capas iniciales capturan bordes y texturas; las capas más profundas codifican formas tumorales complejas y contextos.
Este aprendizaje de extremo a extremo reemplaza las reglas elaboradas a mano con filtros optimizados. Las CNN se adaptan a entradas multimodales (T1, T1c, T2, FLAIR), fusionando automáticamente información a través de secuencias para representaciones más ricas.
El impacto es claro.
- Los modelos profundos segmentan volúmenes 3D completos en segundos, en comparación con los minutos u horas que tomaría hacerlo manualmente.
- Ofrecen resultados consistentes en casos y sitios, aumentando la reproducibilidad.
- Se integran sin problemas con flujos de trabajo multimodales, manejando cualquier combinación de contrastes de MRI sin requerir ajustes personalizados.
Esta velocidad y fiabilidad aceleran los flujos de trabajo clínicos, apoyan análisis radiómicos sólidos y permiten una guía casi en tiempo real en el quirófano.
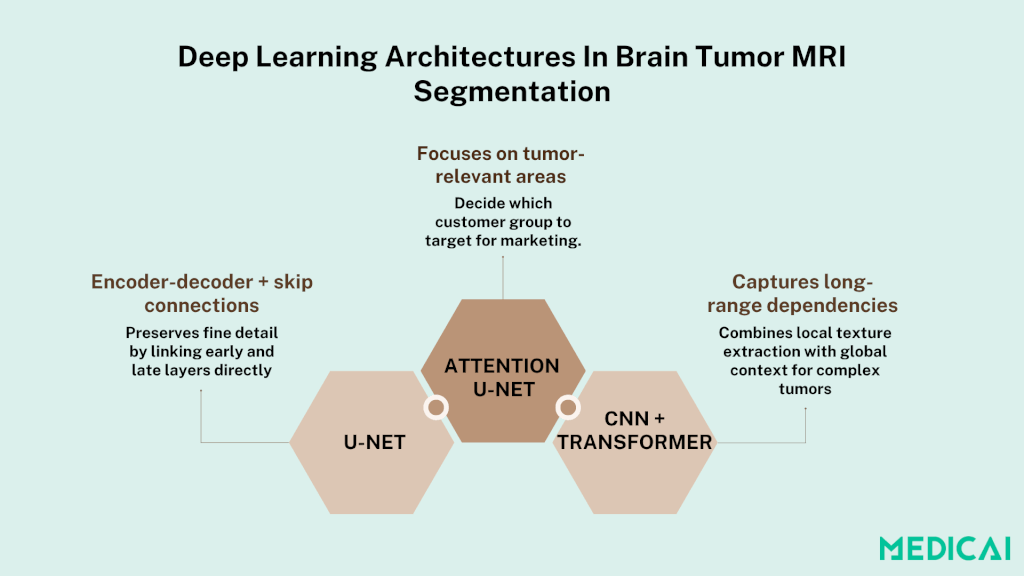
Arquitecturas de Aprendizaje Profundo en la Segmentación de Tumores Cerebrales por MRI
Las arquitecturas de aprendizaje profundo han transformado la segmentación por MRI al aprender características complejas directamente de los datos. Encuentra los modelos clave que impulsan este progreso.
U-Net y sus variantes
U-Net introdujo un diseño de codificador-decodificador simétrico con conexiones de salto que transportan características detalladas de las capas de submuestreo directamente a las capas de sobre-muestreo. Esto permite a la red recuperar detalles espaciales perdidos durante el pooling.
Las capas iniciales aprenden bordes y texturas; las capas más profundas capturan contexto de alto nivel.
3D U-Net extiende este concepto a datos volumétricos al reemplazar convoluciones 2D por 3D. Procesa volúmenes completos de MRI en una sola pasada, preservando la continuidad entre secciones y mejorando la precisión en formas tumorales complejas.
Este enfoque volumétrico exige más memoria pero produce segmentaciones más coherentes a través de las secciones.
U-Net de Atención
U-Net de Atención augments la arquitectura base de U-Net con puertas de atención que re-pesan los mapas de características según su relevancia para las regiones tumorales. La atención espacial destaca áreas clave, mientras que la atención de canal enfatiza los canales de características más informativos.
Este enfoque selectivo permite al modelo ignorar el ruido de fondo y adaptarse a los límites tumorales irregulares. Los estudios han demostrado que los módulos de atención mejoran los índices de Dice, particularmente para lesiones pequeñas o difusas.
Modelos Basados en Transformadores
Los transformadores aportan auto-atención a la imagen médica, calculando relaciones par a par entre todos los voxeles para capturar dependencias a largo alcance y contexto global más allá de los campos receptivos locales de convolución.
Los modelos de transformador puros pueden necesitar muchos datos, por lo que las tuberías híbridas CNN-Transformador primero extraen características de bajo nivel a través de convoluciones y después refinan la segmentación con bloques de transformadores. Los primeros resultados indican que estos híbridos superan a las CNN en tumores heterogéneos y en regímenes con escasos datos.
Segmentación de MRI con Aprendizaje Profundo: Conjuntos de Datos y Preprocesamiento
Datos de alta calidad son la columna vertebral de cualquier tubería de aprendizaje profundo. Un preprocesamiento adecuado convierte imágenes de crudo en entradas confiables para modelos robustos.
Puntos de Referencia Públicos
El desafío de Segmentación de Tumores Cerebrales (BraTS) proporciona un conjunto de datos de MRI multimodal estandarizado, —T1, T1 contrastado (T1c), T2 y FLAIR—cada uno anotado expertamente en subregiones tumorales.—T1, contrast-enhanced T1 (T1c), T2, and FLAIR—each expertly annotated into tumor subregions.
Investigadores de todo el mundo entrenan y evalúan en BraTS para asegurar comparaciones justas e impulsar la innovación.
Pasos de Preprocesamiento
- Normalización de intensidad – Las exploraciones de MRI varían en brillo y contraste, haciendo necesario ajustar estas diferencias. Técnicas como la normalización por puntaje Z o el método de Nyúl reescala las intensidades a un rango común, ayudando a las redes a aprender características consistentes a través de instituciones.
- Eliminación de estructura craneal – Las herramientas automatizadas en MRI eliminan tejido no cerebral (cuero cabelludo, cráneo, grasa), enfocando el modelo en la anatomía cerebral y reduciendo falsos positivos. Este paso utiliza máscaras cerebrales para aislar voxeles relevantes.
- Aumento de datos – Rotaciones aleatorias, escalado, deformaciones elásticas y cambios de intensidad generan ejemplos de entrenamiento variados sobre la marcha. El aumento evita el sobreajuste y mejora la generalización a formas tumorales no vistas y artefactos de imagen.
Entrenamiento basado en parches vs. entrenamiento completo de volúmenes
El entrenamiento basado en parches extrae subvolúmenes más pequeños (p. ej., 80 × 80 × 80 voxels) utilizando ventanas deslizantes. Esto se acomoda a la memoria de la GPU, habilita el sobremuestreo de regiones tumorales raras y equilibra las distribuciones de clases. Sin embargo, puede perder contexto a largo alcance.
El entrenamiento de volumen completo procesa exploraciones de MRI enteras en una sola pasada (como en 3D U-Nets). Preserva la continuidad espacial y el contexto global, llevando a segmentaciones más coherentes a través de las secciones. El compromiso es un mayor uso de memoria y tiempos de entrenamiento más largos.
Juntos, estos puntos de referencia y pasos de preprocesamiento establecen una base para una segmentación de MRI cerebral confiable y reproducible.

Métricas de Evaluación del Aprendizaje Profundo en Segmentación de MRI
Múltiples métricas capturan diferentes aspectos de la calidad de segmentación, proporcionando tanto precisión de volumen como precisión de límites.
Coeficiente de Similitud de Dice (DSC)
El DSC mide la superposición entre la segmentación predicha y la verdad fundamental. Varía de 0 (sin superposición) a 1 (coincidencia perfecta). Un DSC más alto indica mejor acuerdo volumétrico, convirtiéndolo en un punto de referencia principal para tareas de segmentación tumoral.
Distancia de Hausdorff
La métrica captura la desviación de límite más significativa entre los contornos tumorales predichos y reales. Informa la distancia máxima en que cualquier punto en el borde predicho se encuentra del punto más cercano en el borde real.
Valores más bajos denotan una alineación más estrecha de los límites, lo que es crucial para una planificación quirúrgica precisa.
Sensibilidad y Especificidad
La sensibilidad (tasa de verdaderos positivos) mide qué tan bien el modelo detecta voxeles tumorales. La especificidad (tasa de verdaderos negativos) mide cuán precisamente excluye el tejido sano. Equilibrar ambos previene que los modelos favorezcan una clase, garantizando que no dominen la subsegmentación ni la sobrasegmentación.
¿Por qué importan múltiples métricas?
Ninguna métrica única captura todos los aspectos de la calidad de segmentación.
- El DSC destaca en la superposición de volumen pero puede ocultar errores de límite.
- La Distancia de Hausdorff revela desajustes de borde pero ignora la superposición de volumen.
- La sensibilidad y la especificidad destacan problemas de equilibrio de clases.
Usar las cuatro asegura que los modelos funcionen de manera confiable en entornos clínicos, apoyando tanto una estimación precisa de volumen como una delimitación precisa de límites.
Desafíos Clave y Soluciones
La alta variabilidad en los escáneres de MRI y los protocolos puede confundir a los modelos si no se aborda. Desempaquetemos cuatro desafíos centrales y sus soluciones.
Variabilidad del Escáner y del Protocolo
Los datos de MRI provienen de diferentes máquinas, fortalezas de campo y configuraciones de imagen. Estas variaciones desplazan las distribuciones de intensidad y los perfiles de ruido, causando que los modelos entrenados en un centro fallen en otro.
Las técnicas de adaptación de dominio alinean espacios de características a través de diferentes sitios. Las redes de armonización aprenden explícitamente a mapear escaneos de protocolos diversos a una representación común, reduciendo así el «sesgo del escáner» y mejorando el rendimiento entre sitios.
Desequilibrio en la Clase Tumoral
El tejido tumoral a menudo ocupa una pequeña fracción del volumen cerebral, haciendo escasos los ejemplos positivos. Las pérdidas estándar (como la entropía cruzada) sesgan los modelos hacia la predicción de tejido sano.
Funciones de pérdida especializadas como la pérdida focal disminuyen el peso de los negativos fáciles, enfocando el entrenamiento en los voxeles tumorales. Las pérdidas conscientes de límites agregan penalizaciones por colocar incorrectamente los bordes tumorales, mejorando la precisión del contorno en lesiones pequeñas o difusas.
Demandas Computacionales
Los modelos volumétricos, especialmente las 3D U-Nets, requieren una gran memoria de GPU y largos tiempos de entrenamiento. Esto limita los tamaños de lote y retrasa la experimentación.
Arquitecturas eficientes reducen el conteo de parámetros. El entrenamiento de precisión mixta utiliza cálculos de bits más bajos donde es seguro, reduciendo a la mitad el uso de memoria y duplicando el rendimiento sin sacrificar la precisión.
Generalización y Robustez
Los modelos pueden sobreajustarse a las especificidades del sitio de entrenamiento, fallando en datos no vistos.
Una rigurosa validación cruzada por paciente y centro prueba el rendimiento en el mundo real. El entrenamiento multi-institucional, ya sea a través de datos agrupados o aprendizaje federado, crea modelos robustos. Amplias pruebas externas aseguran la fiabilidad antes del uso clínico.
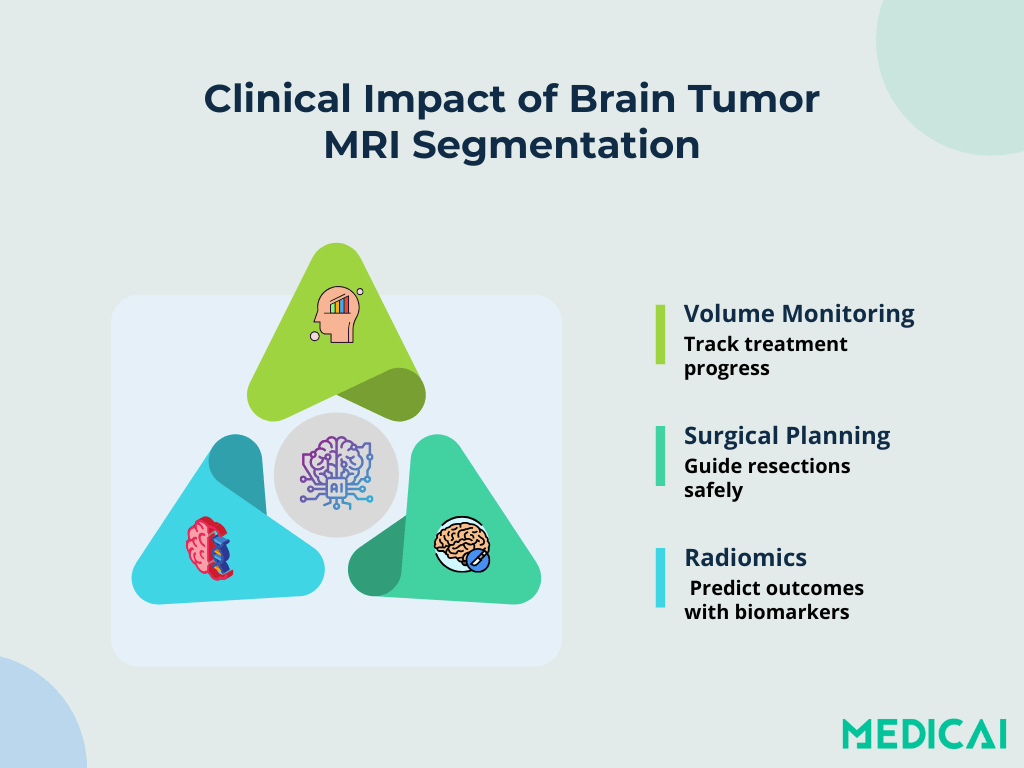
Aplicaciones Clínicas e Impacto
La segmentación respalda tareas clínicas clave en neuro-oncología. Convierte las exploraciones de MRI en percepciones accionables para atención personalizada.
Monitoreo del Crecimiento Volumétrico
Modelos automatizados cuantifican el volumen tumoral a través de escaneos de seguimiento en minutos. Rastrear cambios volumétricos permite a los oncólogos evaluar la respuesta al tratamiento y adaptar los planes de terapia. Las medidas de volumen precisas reducen la dependencia de estimaciones subjetivas y mejoran los estudios longitudinales.
Estimación del Margen Quirúrgico
La clara delineación de los bordes tumorales guía a los neurocirujanos en la planificación de márgenes de resección. Mapas tridimensionales construidos a partir de la segmentación ayudan a equilibrar la extracción del tumor máximo con la preservación del tejido sano.
Esto reduce los déficits postoperatorios y apoya mejores resultados funcionales.
Extracción de Características Radiómicas
Una vez que se definen las regiones tumorales, las tuberías radiómicas extraen características cuantitativas: textura, forma, intensidad, que sirven como biomarcadores de imagen. Estas métricas correlacionan con subtipos moleculares, predicen la supervivencia del paciente y permiten la estratificación del riesgo.
Etiquetas automáticas y consistentes aseguran que los análisis radiómicos se mantengan reproducibles a través de cohortes.
Integración en PACS y Flujos de Trabajo de Tratamiento
Las salidas de aprendizaje profundo se integran perfectamente en los Sistemas de Archivado y Comunicación de Imágenes (PACS) proporcionados por plataformas como Medicai. Las imágenes segmentadas aparecen junto a los escaneos originales en estaciones de trabajo de radiología, permitiendo a los clínicos revisar, ajustar y aprobar contornos sin cambiar de plataforma.
Esta integración acelera los informes, apoya mesas tumorales multidisciplinarias y agiliza el camino desde la imagenología por MRI hacia la intervención.
Conclusión
El aprendizaje profundo ha transformado la segmentación de tumores cerebrales. Los modelos modernos proporcionan mapas rápidos y precisos de los límites tumorales. Reducción de horas de trabajo manual a segundos. Las tuberías automatizadas apoyan la planificación del tratamiento, el descubrimiento de biomarcadores radiómicos y la guía quirúrgica.
La plataforma de Medicai trae estas herramientas directamente a tu flujo de trabajo. Se integra con tu configuración de PACS y ofrece resultados consistentes en todos los casos.
Artículos relacionados



¡Pongámonos en contacto!
Descubra cómo Medicai puede ayudarle a fortalecer su consulta y mejorar la experiencia de sus pacientes. ¿Listo para comenzar su viaje?
Reserve una demostración gratuita