Cómo el Aprendizaje Profundo Revoluciona la Segmentación de MRI Cardíaca
¿Qué pasaría si tu próximo informe de resonancia magnética cardíaca llega antes de que termines tu café?
La segmentación automática y totalmente profunda combina un detector de ROI impulsado por CNN, una estructura basada en U-Net y un refinamiento de modelo deformable para ofrecer máscaras de cámara precisas en segundos. El resultado son contornos de calidad clínica, puntajes de Dice superiores a 0.90 y mediciones de fracción de eyección reproducibles.
Descubre la arquitectura, las recetas de entrenamiento, los resultados de referencia y las aplicaciones reales que hacen posible la segmentación rápida y confiable de resonancias magnéticas cardíacas.

¿Por qué el Aprendizaje Profundo Está Revolucionando la Resonancia Magnética Cardíaca?
La resonancia magnética cardíaca tradicionalmente requiere que los expertos tracen manualmente los bordes de las cámaras, un proceso lento que puede tomar de 15 a 30 minutos por escaneo y varía entre lectores. Estas inconsistencias pueden impactar significativamente en métricas clave, como la fracción de eyección y el volumen sistólico, que son cruciales para tomar decisiones de tratamiento informadas.
Segmentación de MRI mediante aprendizaje profundo invierte este flujo de trabajo.
Las redes convolucionales aprenden a identificar las estructuras del corazón directamente a partir de los datos de imagen. Una vez entrenadas, producen contornos precisos en segundos. Esta velocidad permite informes el mismo día, liberando a los especialistas para que se concentren en casos complejos en lugar de en delineaciones rutinarias.
Más allá de la velocidad, la segmentación automatizada reduce la variabilidad entre observadores. Estudios muestran que los modelos de aprendizaje profundo logran puntajes de Dice superiores a 0.90 para ambos ventrículos, derecho e izquierdo, a la par y a menudo superando a los de los expertos humanos. Mediciones consistentes generan confianza en los clínicos y apoyan un monitoreo confiable de la progresión de la enfermedad.
Finalmente, las redes modernas se adaptan a diversos protocolos de imagen. A través de la augmentación de datos y un entrenamiento robusto en conjuntos de datos de múltiples proveedores, toleran diferencias en la marca del escáner, la fuerza del campo y los parámetros de adquisición. Esta generalizabilidad significa que el mismo modelo puede servir a hospitales en todo el mundo sin una re-tuning exhaustiva.
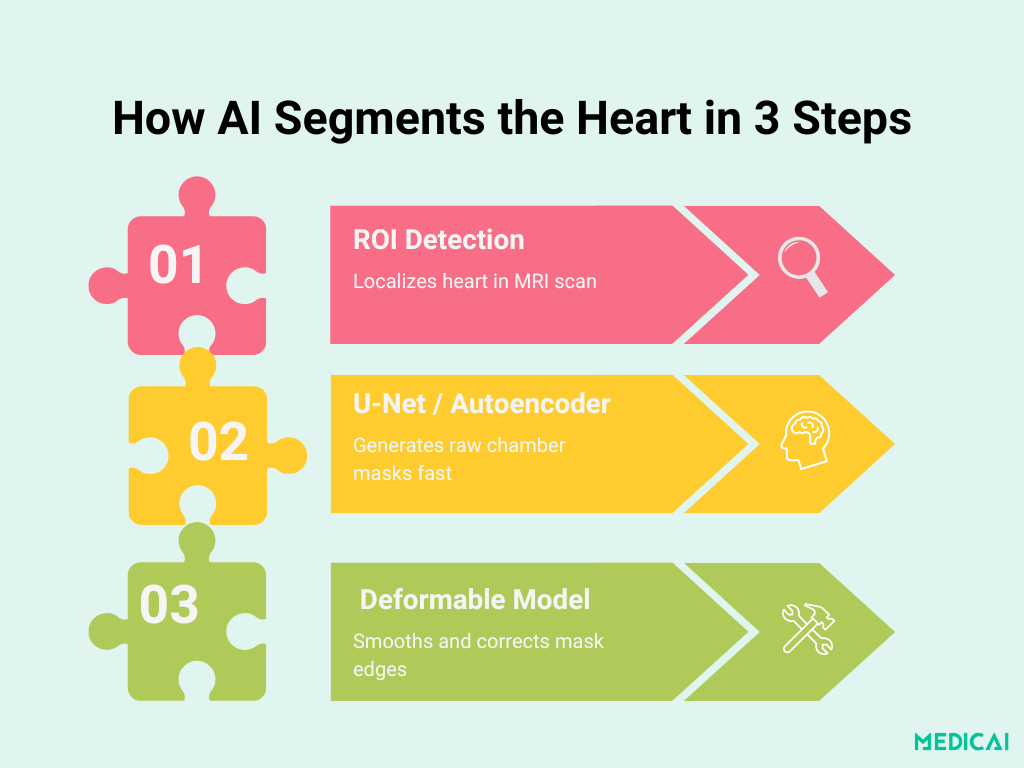
Anatomía del Pipeline: De ROI a Contorno Final
La segmentación de cámaras basada en aprendizaje profundo se desarrolla en tres etapas claras. Cada paso se basa en el anterior para ofrecer máscaras rápidas, precisas y anatómicamente consistentes.
Localización de ROI del Corazón con CNNs
La primera etapa utiliza una red neuronal convolucional ligera para identificar la región cardíaca en cada sección de MRI. Al entrenar con imágenes en bruto con cuadros delimitadores anotados manualmente, la red aprende a recortar la anatomía irrelevante (como los pulmones y la pared torácica) y concentrarse únicamente en las cámaras cardíacas.
Esta segmentación específica “Región de Interés” (ROI) reduce la complejidad downstream y aumenta tanto la velocidad como la precisión.
Backbone de Segmentación: U-Net & Autoencoders Apilados
Una vez extraída la ROI, una red de segmentación delimita los límites de las cámaras:
- Variantes de U-Net: Muchos estudios de alto rango emplean una arquitectura U-Net 2D, caracterizada por un camino de codificador-decodificador que utiliza convoluciones 3×3, normalización por lotes, activaciones ReLU y conexiones de salto para preservar el contexto espacial. Las profundidades de filtro generalmente progresan de 32 a 64 a 128 a 256, equilibrando la captura de detalles contra el costo computacional.
- Autoencoder Apilado (Método del Póster): El pipeline del póster utiliza en cambio un autoencoder apilado entrenado para reproducir la entrada de ROI, aprendiendo implícitamente los priors de forma de las cámaras. Su cuello de botella obliga a la red a destilar características cardíacas esenciales, produciendo una máscara inicial a nivel de píxeles que alimenta la etapa de refinamiento.
Fusión de Modelo Deformable para Bordes Impecables
Las máscaras de aprendizaje profundo en bruto pueden ser ligeramente irregulares o desalineadas en bordes complejos. Para asegurar la plausibilidad anatómica, el contorno inicial se integra en un modelo deformable clásico (contorno activo):
- Inicialización: La salida del autoencoder o U-Net proporciona la curva inicial.
- Minimización de Energía: Términos de forma e intensidad guían el contorno para seguir de cerca los bordes reales de la cámara.
- Suavizado de Salida: La máscara final es tanto suave como adherente a la anatomía precisa, corrigiendo artefactos menores de aprendizaje profundo sin intervención manual.
Este diseño de tres etapas combina la velocidad y el poder de aprendizaje de las CNNs con el rigor geométrico de los modelos deformables.

Entrenando la Red: Recetas para una Segmentación Fuerte
Construir un modelo que generaliza entre pacientes y escáneres depende de la elección cuidadosa de funciones de pérdida, aumentación inteligente y protocolos de validación rigurosos.
Pérdidas Inteligentes: Dice se Encuentra con Entropía Cruzada
La entropía cruzada pura optimiza la precisión a nivel de píxeles, pero puede tener problemas con el desequilibrio de clases cuando las cámaras ocupan solo una fracción de la imagen. La pérdida de Dice maximiza la superposición pero puede ser inestable al principio del entrenamiento. Combinarlos produce lo mejor de ambos mundos:
- Entropía Cruzada Ponderada: penaliza píxeles mal clasificados, manteniendo la red centrada en la corrección por voxel.
- Pérdida de Dice: maximiza directamente la superposición entre la predicción y la verdad de base, mejorando así la delineación del contorno.
- Regulación L2: Domina los pesos excesivamente grandes para lograr una convergencia más suave.
Los estudios informan que esta pérdida híbrida supera a cualquiera de los componentes por separado, aumentando los puntajes promedio de Dice en conjuntos de datos de MRI retenidos en 2 a 3 puntos porcentuales.
Aumentación de Datos para Superar la Variabilidad del Escáner
Los protocolos de MRI cardíaca varían drásticamente: fuerzas de campo, grosores de corte, planos de imagen, por lo que las aumentaciones simulan esta diversidad.
- Geométricos Transformaciones: rotaciones (por ejemplo, múltiplos de 60°), escalado, traducciones, volteos
- Deformaciones Elásticas: los estiramientos suaves aleatorios mimetizan la variabilidad anatómica y el movimiento respiratorio.
- Desplazamientos de Intensidad: jitter de contraste y brillo cuenta para las diferencias en la calibración del escáner.
Aumentar sobre la marcha asegura que el modelo vea una variedad casi infinita de ejemplos, reduciendo drásticamente el sobreajuste y mejorando el rendimiento entre proveedores.
Estrategia de Optimización & Validación
Un régimen de entrenamiento intenso asegura que realmente estés aprendiendo la anatomía del corazón, no peculiaridades del conjunto de datos.
- Optimizadores: Adam o SGD con una tasa de aprendizaje inicial de ~1×10⁻⁴, reducida a la mitad cada 10–20 épocas para refinar los pesos.
- Detención Temprana: monitorea el Dice de validación; detiene el proceso cuando las mejoras se estancan durante 10 épocas consecutivas.
- Validación Cruzada: divisiones de 5 pliegues en conjuntos de referencia (ACDC, MICCAI RV/LV) para evaluar la estabilidad y evitar divisiones afortunadas.
Estos elecciones equilibran la velocidad de convergencia y la generalización, proporcionando contornos de calidad clínica en condiciones del mundo real.
Demostrando Desempeño: Métricas que Importan
Evaluar la segmentación de MRI la calidad depende de tres métricas clave. Cada una captura un aspecto distinto de cuán de cerca la máscara automática coincide con las delineaciones de expertos.
Coeficiente de Similitud de Dice (DSC)
El DSC mide la superposición volumétrica entre las máscaras predicha y de verdad. Los valores oscilan entre 0 (sin superposición) y 1 (superposición perfecta). Los modelos más avanzados logran rutinariamente DSC > 0.90 para ambos ventrículos izquierdo y derecho, situando su precisión a la par con la de los lectores expertos.
Distancia de Hausdorff (HD)
La HD cuantifica el error de límite en el peor de los casos en milímetros, definido como la mayor distancia desde cualquier punto en un contorno hasta el punto más cercano en el otro. Una HD baja (< 10 mm) indica que la máscara sigue de manera precisa los bordes anatómicos finos.
Informar tanto la media como la desviación estándar de la HD ayuda a revelar la consistencia entre escaneos de pacientes.
Correlación de Volumen (R)
Los coeficientes de correlación se utilizan para comparar las mediciones automáticas y manuales del volumen end-diastólico (EDV), volumen end-sistólico (ESV) y fracción de eyección (EF). Altos valores de R (≥ 0.99) indican que el modelo produce métricas cuantitativas equivalentes clínicamente, asegurando confianza en los índices funcionales posteriores.
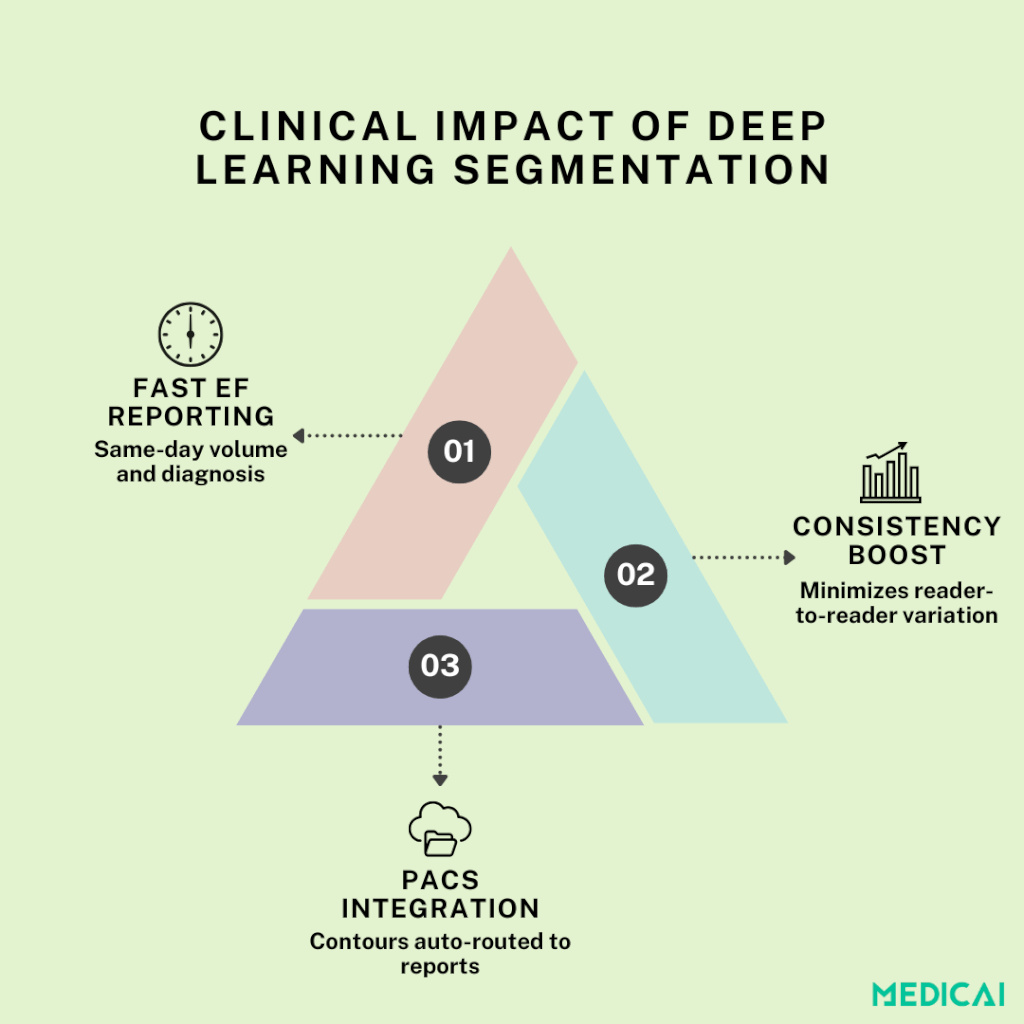
Impacto Clínico: Más Rápido, Consistente, Escalable
La segmentación de cámaras impulsada por aprendizaje profundo transforma los flujos de trabajo clínicos en tres formas clave.
Informe Automatizado de Fracción de Eyección
Al entregar volúmenes ventriculares precisos en cuestión de segundos, la segmentación impulsada por IA permite el cálculo el mismo día del volumen end-diastólico (EDV), volumen end-sistólico (ESV) y fracción de eyección (EF). Este rápido retorno acelera el diagnóstico y apoya ajustes de tratamiento oportunos sin demoras de trazado manual.
Minimización de la Variabilidad entre Observadores
La delineación manual tradicional sufre de diferencias entre lectores: pequeños cambios en los contornos pueden traducirse en discrepancias significativas en la fracción de eyección.
Los modelos de aprendizaje profundo logran puntajes de Dice de ≥ 0.90 y correlaciones de volumen de ≥ 0.99, asegurando mediciones consistentes y aumentando la confianza del clínico en el monitoreo del paciente.
Integración PACS/RIS Sin Costuras
Una vez entrenado, el pipeline puede ser incrustado directamente en Sistemas de Archivo y Comunicación de Imágenes (PACS) proporcionados por plataformas como Medicai o Sistemas de Información Radiológica (RIS).
El procesamiento completamente automático no requiere interacción del usuario, dirigiendo contornos finalizados e informes cuantitativos al registro médico electrónico. Agilizan las cargas de trabajo de radiología.
Superando Obstáculos: Limitaciones & Soluciones
A pesar de su promesa, la IA en MRI los pipelines de segmentación deben abordar tres desafíos persistentes para lograr una adopción clínica generalizada.
Variabilidad del Escáner
Las diferencias en la fuerza del campo, secuencias específicas del proveedor y el grosor del corte pueden degradar el rendimiento del modelo.
Las soluciones incluyen una extensa aumentación de datos durante el entrenamiento (rotaciones, jitter de intensidad, deformaciones elásticas) y un ajuste fino en pequeños lotes de escaneos de nuevos sitios para adaptarse a protocolos locales.
Patologías Raras (p.ej., Hipertrofia)
Condiciones poco comunes como la hipertrofia septal asimétrica o malformaciones congénitas pueden no aparecer en conjuntos de entrenamiento estándar. Esto puede llevar a subsegmentación o distorsiones de forma.
Las estrategias de mitigación incluyen colecciones de casos específicas, aumentación sintética para anatomías extremas y uso de estimaciones de incertidumbre para señalar salidas de baja confianza para revisión.
Cuellos de Botella en la Anotación de Datos
Los contornos manuales de alta calidad son intensivos en mano de obra y costosos, limitando el tamaño de los corpus de entrenamiento.
Métodos como el aprendizaje semi-supervisado, el aprendizaje federado y el aprendizaje activo pueden reducir la necesidad de datos etiquetados aprovechando escaneos no marcados, compartiendo actualizaciones sin transferir datos y enfocándose en casos clave.
Conclusión
El aprendizaje profundo automatizado permite una segmentación rápida y precisa de las cámaras cardíacas en resonancias magnéticas cardiacas, proporcionando contornos precisos en segundos. Combina CNN para localización, U-Net para procesamiento y modelos deformables para refinamiento para proporcionar resultados confiables a los clínicos.
Con la integración de PACS lista para usar de Medicai, actualizaciones de modelo federadas y tableros explicativos, puedes desplegar este pipeline de vanguardia al instante. Con nosotros, puedes ofrecer atención cardíaca más rápida e inteligente a cada paciente.
Artículos relacionados



¡Pongámonos en contacto!
Descubra cómo Medicai puede ayudarle a fortalecer su consulta y mejorar la experiencia de sus pacientes. ¿Listo para comenzar su viaje?
Reserve una demostración gratuita