Segmentation d'images IRM de tumeurs cérébrales utilisant des techniques d'apprentissage profond
Imaginez réduire des heures de segmentation manuelle de l’IRM cérébrale à quelques secondes.
Les limites des tumeurs cérébrales émergent automatiquement, et l’apprentissage profond rend cela possible. Cela apporte précision, rapidité et cohérence aux flux de travail en neuro-oncologie.
L’apprentissage profond exploite les CNN, les U-Nets avec attention et les hybrides de transformateurs pour segmenter automatiquement des IRM multimodales. Ces modèles surclassent les méthodes classiques en termes de vitesse, d’exactitude et de reproductibilité, permettant une délimitation précise des limites de la tumeur pour une utilisation clinique dans divers contextes.
Découvrez la segmentation des images IRM des tumeurs cérébrales à l’aide des techniques d’apprentissage profond : architectures de base, ensembles de données et impacts cliniques.

Qu’est-ce que la segmentation des tumeurs cérébrales basée sur l’IRM ?
La segmentation des tumeurs cérébrales basée sur l’IRM divise les IRM en régions étiquetées, séparant le tissu tumoral des structures cérébrales normales. Chaque voxel est regroupé par des caractéristiques communes, y compris –
- Intensité
- Texture
- Limites
Ils créent une carte claire des sous-régions tumorales.
Ce regroupement automatisé remplace les conjectures par des étiquettes précises et basées sur les données. La segmentation est la première étape critique pour toute analyse ultérieure.
Dans la segmentation manuelle, des radiologues experts dessinent laborieusement les contours des tumeurs sur chaque coupe de l’image. Ce traçage coupe par coupe peut prendre des heures par cas et varie selon le lecteur.
Les modèles d’apprentissage profond automatisés apprennent à prédire ces contours en quelques secondes. Les outils semi-automatiques nécessitent encore quelques corrections de l’utilisateur ; les réseaux entièrement automatiques livrent des prédictions de bout en bout sans intervention manuelle.
Une enquête souligne que les réseaux profonds surpassent les méthodes classiques en termes de rapidité et de cohérence.
Une segmentation précise assure de meilleurs soins.
- Elle fournit des mesures de volume précises pour la planification de la radiothérapie.
- Elle standardise les régions pour l’extraction de caractéristiques radiomiques, produisant des biomarqueurs fiables.
- Dans la salle d’opération, des cartes tumorales 3D claires guident les chirurgiens pour maximiser la résection tout en préservant le tissu sain.
Ainsi, la segmentation automatisée accélère les flux de travail et soutient la neuro-oncologie personnalisée.
Pourquoi l’apprentissage profond pour la segmentation des images IRM des tumeurs cérébrales
Les techniques de traitement d’images classiques, telles que le seuillage et la croissance de région, segmentent les tumeurs en regroupant des pixels ayant des intensités similaires ou une proximité spatiale. Elles rencontrent des difficultés lorsque les limites de la tumeur sont floues ou lorsque l’intensité chevauche le tissu sain.
Ces méthodes nécessitent souvent un réglage manuel des seuils pour chaque patient et échouent en présence de bruit d’IRM ou de paramètres de scanner variables.
Les réseaux de neurones convolutionnels (CNN) surmontent ces limites en apprenant les hiérarchies de caractéristiques directement à partir des données. Les couches précoces capturent les bords et les textures ; les couches plus profondes codent des formes tumoral complexes et du contexte.
Cet apprentissage de bout en bout remplace les règles artisanales par des filtres optimisés. Les CNN s’adaptent à des entrées multimodales (T1, T1c, T2, FLAIR), fusionnant automatiquement les informations à travers les séquences pour des représentations plus riches.
L’impact est clair.
- Les modèles profonds segmentent des volumes 3D complets en quelques secondes, par rapport aux minutes ou aux heures qu’il faudrait pour le faire manuellement.
- Ils livrent des résultats cohérents à travers les cas et les sites, augmentant la reproductibilité.
- Ils s’intègrent parfaitement dans des pipelines multimodaux, gérant n’importe quelle combinaison de contrastes IRM sans nécessiter d’ajustements spécifiques.
Cette rapidité et cette fiabilité accélèrent les flux de travail cliniques, soutiennent des analyses radiomiques solides, et permettent une guidance presque en temps réel dans la salle d’opération.
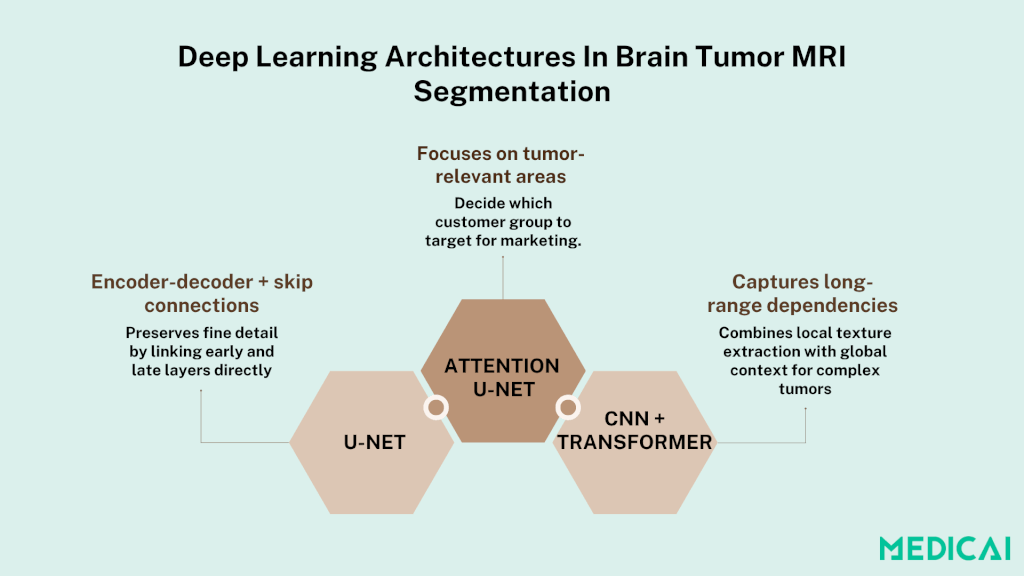
Architectures d’apprentissage profond dans la segmentation des tumeurs cérébrales IRM
Les architectures d’apprentissage profond ont transformé la segmentation IRM en apprenant des caractéristiques complexes directement à partir des données. Trouvez les modèles clés qui conduisent ce progrès.
U-Net et ses variantes
U-Net a introduit un design d’encodeur-décodeur symétrique avec des connexions de saut qui transfèrent les caractéristiques fines des couches de sous-échantillonnage directement vers les couches de sur-échantillonnage. Cela permet au réseau de récupérer des détails spatiaux perdus lors du pooling.
Les couches précoces apprennent les bords et les textures ; les couches plus profondes capturent le contexte de haut niveau.
Le 3D U-Net étend ce concept aux données volumétriques en remplaçant les convolutions 2D par des convolutions 3D. Il traite l’ensemble des volumes IRM en un seul passage, préservant la continuité inter-coupes et augmentant la précision sur des formes tumorales complexes.
Cette approche volumétrique exige plus de mémoire mais produit des segmentations plus cohérentes à travers les coupes.
Attention U-Net
Attention U-Net augmente l’arrière-plan U-Net avec des portes d’attention qui réajustent les cartes de caractéristiques en fonction de leur pertinence pour les régions tumorales. L’attention spatiale met en évidence des zones clés, tandis que l’attention de canal accentue les canaux de caractéristiques les plus informatifs.
Cette concentration sélective permet au modèle d’ignorer le bruit de fond et de s’adapter aux limites tumorales irrégulières. Des études ont montré que les modules d’attention améliorentles scores de Dice, en particulier pour des lésions petites ou diffuses.
Modèles basés sur les transformateurs
Les transformateurs apportent l’attention auto-dirigée à l’imagerie médicale, calculant les relations par paires entre tous les voxels pour capturer les dépendances à long terme et le contexte global au-delà des champs récepteurs locaux convolutionnels.
Les modèles de transformateurs purs peuvent être voraces en données, donc les pipelines hybrides CNN-Transformateur extraient d’abord des caractéristiques de bas niveau via des convolutions, puis affinent la segmentation avec des blocs de transformateur. Les premiers résultats indiquent que ces hybrides surpassent les CNN sur des tumeurs hétérogènes et dans des régimes avec peu de données.
Segmentation IRM Apprentissage profond : Ensembles de données et Prétraitement
Des données de haute qualité sont l’épine dorsale de tout pipeline d’apprentissage profond. Un prétraitement approprié transforme les IRM brutes en entrées fiables pour des modèles robustes.
Références publiques
Le défi de segmentation de tumeurs cérébrales (BraTS) fournit un ensemble de données IRM multimodal standardisé, ensemble de données IRM multimodal—T1, T1 amélioré par contraste (T1c), T2 et FLAIR—chacune annotée de manière experte en sous-régions tumorales.
Des chercheurs du monde entier s’entraînent et évaluent sur BraTS pour garantir des comparaisons équitables et stimuler l’innovation.
Étapes de prétraitement
- Normalisation de l’intensité – Les IRM varient en luminosité et en contraste, rendant nécessaire l’ajustement de ces différences. Des techniques comme la normalisation par score Z ou la méthode de Nyúl re-échelonnent les intensités sur un intervalle commun, aidant les réseaux à apprendre des caractéristiques cohérentes à travers les institutions.
- Élimination du crâne – Des outils automatisés en IRM suppriment les tissus non cérébraux (scalp, crâne, graisse), concentrant le modèle sur l’anatomie cérébrale et réduisant les faux positifs. Cette étape utilise des masques cérébraux pour isoler les voxels pertinents.
- Augmentation des données – Des rotations aléatoires, des mises à l’échelle, des déformations élastiques et des changements d’intensité génèrent des exemples d’entraînement variés à la volée. L’augmentation prévient le surapprentissage et renforce la généralisation à des formes tumorales invisibles et des artefacts d’imagerie.
Entraînement par patch vs Entraînement de volume complet
L’entraînement par patch extrait de plus petits sous-volumes (par exemple, 80 × 80 × 80 voxels) en utilisant des fenêtres glissantes. Cela s’adapte à la mémoire GPU, permet le suréchantillonnage de régions tumorales rares et équilibre les distributions de classes. Cependant, cela peut faire perdre le contexte à long terme.
L’entraînement de volume complet traite l’ensemble des IRM en un seul passage (comme dans les 3D U-Nets). Il préserve la continuité spatiale et le contexte global, conduisant à des segmentations plus cohérentes à travers les coupes. Le compromis est une utilisation de mémoire plus élevée et des temps d’entraînement plus longs.
Ensemble, ces références et étapes de prétraitement établissent une fondation pour une segmentation IRM cérébrale modèles fiables et reproductibles.

Évaluation des métriques d’apprentissage profond pour la segmentation IRM
Plusieurs métriques capturent différents aspects de la qualité de segmentation, fournissant à la fois des mesures de volume et de précision des bordures.
Coefficient de similarité de Dice (DSC)
Le DSC mesure la superposition entre la segmentation prédite et la vérité de terrain. Il varie de 0 (pas de superposition) à 1 (correspondance parfaite). Un DSC plus élevé indique un meilleur accord volumétrique, en faisant une référence principale pour les tâches de segmentation tumorale.
Distance de Hausdorff
La métrique capture la plus significative des déviations de contours entre les contours tumoraux prédits et réels. Elle rapporte la distance maximale entre n’importe quel point sur la bordure prédite et le point le plus proche sur la bordure réelle.
Des valeurs plus faibles indiquent un meilleur alignement des limites, ce qui est crucial pour une planification chirurgicale précise.
Sensibilité et spécificité
La sensibilité (taux de vrais positifs) évalue à quel point le modèle détecte les voxels tumoraux. La spécificité (taux de vrais négatifs) mesure à quel point il exclut correctement le tissu sain. L’équilibre des deux empêche les modèles de favoriser une classe, garantissant qu’aucune sous-segmentation ni sur-segmentation ne domine.
Pourquoi plusieurs métriques sont-elles importantes ?
Aucune métrique unique ne capture tous les aspects de la qualité de segmentation.
- Le DSC excelle dans le chevauchement des volumes mais peut masquer des erreurs de contour.
- La distance de Hausdorff révèle des désaccords de bord mais ignore le chevauchement des volumes.
- La sensibilité et la spécificité mettent en évidence les problèmes d’équilibre des classes.
L’utilisation des quatre garantit que les modèles fonctionnent de manière fiable dans des contextes cliniques, soutenant à la fois une estimation précise des volumes et une délimitation précise des contours.
Défis clés et solutions
Une grande variabilité dans les scanners IRM et les protocols peut perturber les modèles si elle n’est pas abordée. Détaillons quatre défis de base et leurs solutions.
Variabilité des scanners et des protocoles
Les données IRM proviennent de différentes machines, forces de champ, et réglages d’imagerie. Ces variations déplacent les distributions d’intensité et de bruit, provoquant un échec des modèles formés sur un centre à fonctionner sur un autre.
Les techniques d’adaptation de domaine alignent les espaces de caractéristiques à travers différents sites. Les réseaux de harmonisation apprennent explicitement à mapper les scans de protocoles divers dans une représentation commune, réduisant ainsi le « biais de scanner » et améliorant la performance inter-sites.
Déséquilibre des classes tumorales
Le tissu tumoral occupe souvent une fraction infime du volume cérébral, rendant les exemples positifs rares. Les pertes standard (comme l’entropie croisée) biaisent alors les modèles vers la prédiction du tissu sain.
Des fonctions de perte spécialisées telles que la perte focale diminuent le poids des négatifs faciles, se concentrant sur l’entraînement des voxels tumoraux. Les pertes sensibles aux limites ajoutent des pénalités pour le placement incorrect des bords tumoraux, améliorant la précision des contours dans les lésions petites ou diffuses.
Exigences computationnelles
Les modèles volumétriques, en particulier les 3D U-Nets, nécessitent une grande mémoire GPU et des temps d’entraînement longs. Cela limite les tailles de lot et ralentit l’expérimentation.
Des architectures efficaces réduisent le nombre de paramètres. L’entraînement en précision mixte utilise des calculs à plus faible nombre de bits où c’est sûr, réduisant de moitié l’utilisation de la mémoire et doublant le débit sans sacrifier la précision.
Généralisation et robustesse
Les modèles peuvent sur-apprendre aux spécificités du site d’entraînement, échouant sur des données non vues.
Une validation croisée rigoureuse par patient et centre teste la performance dans le monde réel. Un entraînement multi-institutionnel, que ce soit par des données regroupées ou par apprentissage fédéré, crée des modèles robustes. Des tests externes étendus garantissent la fiabilité avant utilisation clinique.
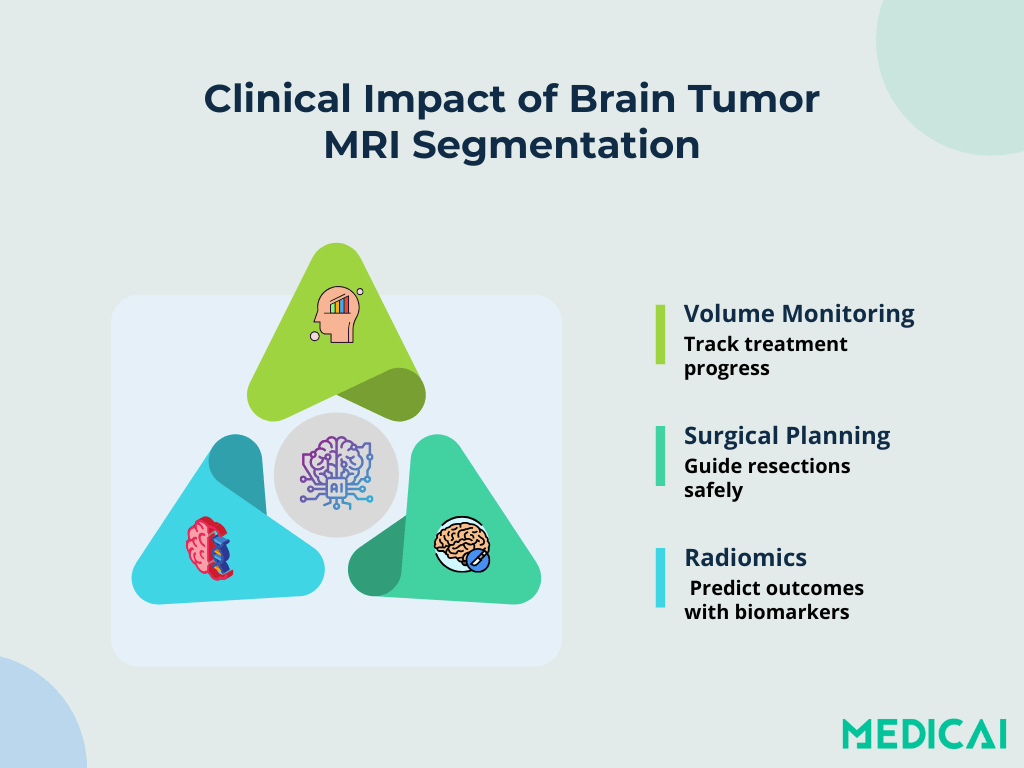
Applications cliniques et impact
La segmentation sous-tend des tâches cliniques clés en neuro-oncologie. Elle transforme des IRM brutes en informations exploitables pour des soins personnalisés.
Suivi de la croissance volumétrique
Des modèles automatisés quantifient le volume tumoral à travers des IRM de suivi en quelques minutes. Suivre les changements volumétriques permet aux oncologues d’évaluer la réponse au traitement et d’adapter les plans de thérapie. Des mesures de volume précises réduisent la dépendance à des estimations subjectives et renforcent les études longitudinales.
Estimation des marges chirurgicales
Une délimitation claire des bords tumoraux guide les neurochirurgiens dans la planification des marges de résection. Des cartes tridimensionnelles construites à partir de la segmentation aident à équilibrer le retrait maximal de la tumeur tout en préservant le tissu sain.
Cela réduit les déficits postopératoires et favorise de meilleurs résultats fonctionnels.
Extraction de caractéristiques radiomiques
Une fois les régions tumorales définies, des pipelines radiomiques extraient des caractéristiques quantitatives – texture, forme, intensité – qui servent de biomarqueurs d’imagerie. Ces métriques sont corrélées avec des sous-types moléculaires, prédisent la survie des patients et permettent la stratification des risques.
Des étiquettes automatisées et cohérentes garantissent que les analyses radiomiques restent reproductibles à travers les cohortes.
Intégration dans les systèmes PACS et les flux de travail de traitement
Les résultats de l’apprentissage profond alimentent sans effort les Systèmes d’Archivage et de Communication d’Images (PACS) fournis par des plateformes comme Medicai. Les images segmentées apparaissent aux côtés des scans bruts dans les stations de travail de radiologie, permettant aux cliniciens de réviser, ajuster et approuver les contours sans changer de plateforme.
Cette intégration accélère le reporting, soutient des commissions multidisciplinaires sur les tumeurs et rationalise le chemin de l’imagerie IRM à l’intervention.
Conclusion
L’apprentissage profond a redéfini la segmentation des tumeurs cérébrales. Les modèles modernes fournissent des cartes rapides et précises des limites tumorales. Ils réduisent des heures de travail manuel à quelques secondes. Les pipelines automatisés soutiennent la planification du traitement, la découverte de biomarqueurs radiomiques et la guidance chirurgicale.
La plateforme de Medicai intègre ces outils directement dans votre flux de travail. Elle s’intègre à votre configuration PACS et fournit des résultats cohérents à travers les cas.
Articles connexes



Contactez-nous!
Découvrez comment Medicai peut vous aider à renforcer votre cabinet et à améliorer l’expérience de vos patients. Prêt à vous lancer?
Réservez une démonstration gratuite