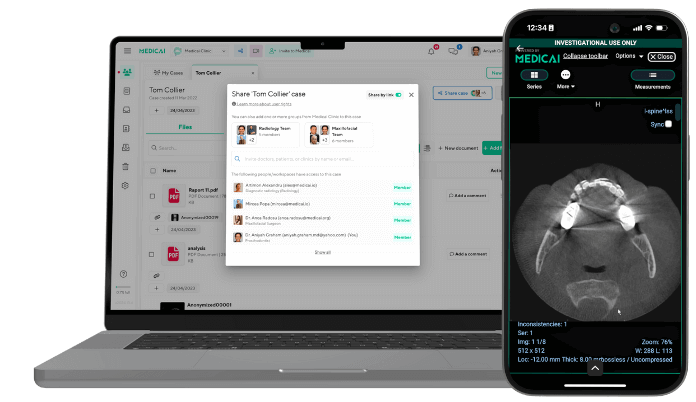
Cum Revoluționează Învățarea Profundă Segmentarea RMN-ului Cardiac
Ce se întâmplă dacă următorul raport de RMN cardiac ajunge înainte să termini cafeaua?
Segmentarea complet automatizată bazată pe învățare profundă combină un detector ROI alimentat de CNN, o arhitectură bazată pe U-Net și un model deformabil de refinare pentru a oferi măști pixel-perfect ale camerelor în câteva secunde. Rezultatul este contururi de grad clinician, scoruri Dice peste 0,90 și măsurători reproduceabile ale fracției de ejecție.
Descoperiți arhitectura, rețetele de antrenament, rezultatele de referință și aplicațiile din lumea reală care fac din segmentarea rapidă și fiabilă a RMN-ului cardiac o realitate.

De ce Învățarea Profundă Revoluționează RMN-ul Cardiac?
RMN-ul cardiac, în mod tradițional, necesită experți pentru a urmări manual marginea camerelor, un proces lent care poate dura 15-30 de minute per scanare și variază între cititori. Aceste inconsistențe pot afecta semnificativ metricile cheie, cum ar fi fracția de ejecție și volumul de sânge, care sunt cruciale pentru decizii informate în tratament.
Segmentarea RMN-ului prin învățare profundă întoarce acest flux de lucru pe dos.
Rețelele convoluționale învață să identifice structurile cardiace direct din datele de imagine. Odată antrenate, acestea produc contururi pixel-perfect în câteva secunde. Această viteză permite emiterea de rapoarte în aceeași zi, eliberând specialiștii să se concentreze pe cazuri complexe în loc de contururi de rutină.
Dincolo de viteză, segmentarea automată reduce variabilitatea inter-observator. Studiile arată că modelele de învățare profundă obțin scoruri Dice peste 0,90 atât pentru ventriculul stâng, cât și pentru cel drept—pe aceeași linie cu, și adesea depășind, cele ale experților umani. Măsurătorile constante construiesc încrederea clinicianului și susțin monitorizarea fiabilă a progresiei bolii.
În cele din urmă, rețelele moderne se adaptează la diverse protocoale de imagistică. Prin augmentarea datelor și antrenamentul robust pe seturi de date multi-vendor, acestea tolerează diferențele în marca scannerului, intensitatea câmpului și parametrii de achiziție. Această generalizabilitate înseamnă că același model poate servi spitale din întreaga lume fără o recalibrare minuțioasă.
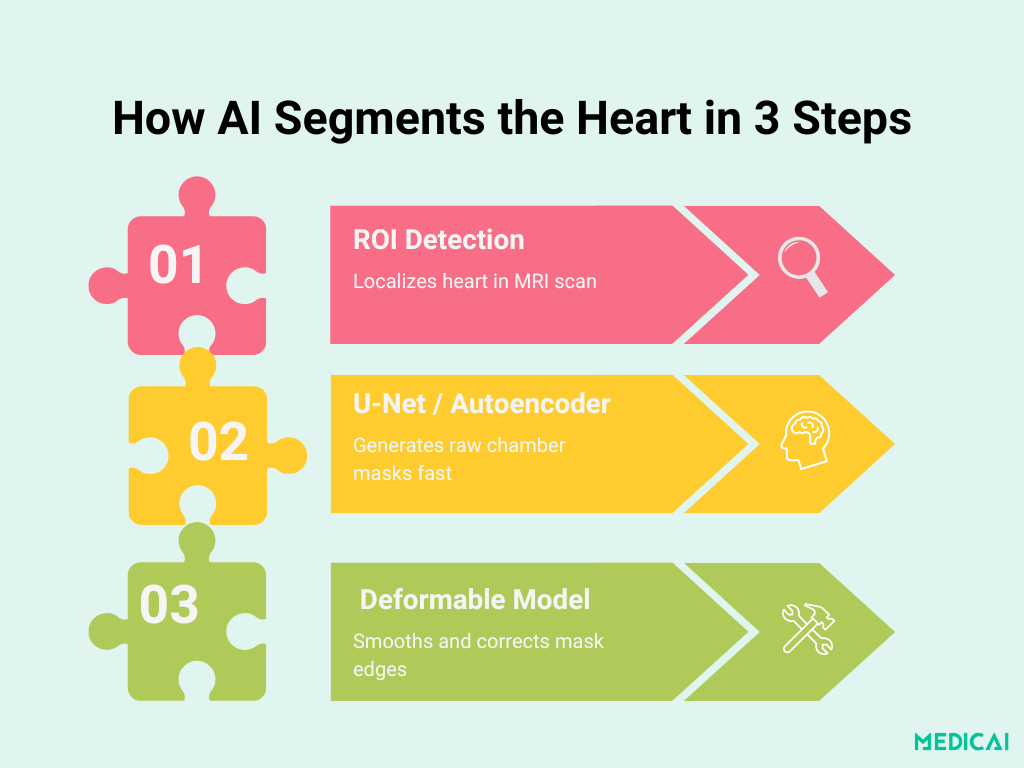
Anatomia Pipeline-ului: De la ROI la Conturul Final
Segmentarea camerelor bazată pe învățare profundă se desfășoară în trei etape clare. Fiecare pas se bazează pe precedent pentru a oferi măști rapide, precise și consistent anatomice.
Localizarea ROI a Inimii cu CNN-uri
Prima etapă folosește o rețea neurală convoluțională ușoară pentru a localiza regiunea inimii în fiecare felie de RMN. Prin antrenamentul pe imagini brute cu boxe de delimitare annotate manual, rețeaua învață să taie anatomia irelevantă (precum plămânii și peretele toracic) și să se concentreze exclusiv pe camerele cardiace.
Această țintire „Regiune de Interes” (ROI) reducerea crop-ului complexității descendente și îmbunătățește atât viteza cât și acuratea.
Structura de Segmentare: U-Net & Auto-Encoder-uri Stivuite
Odată ce ROI a fost extras, o rețea de segmentare delimitează limitele camerelor:
- Variante U-Net: Multe studii de top folosesc o arhitectură U-Net 2D, caracterizată printr-un parcurs encoder–decoder care utilizează convoluții de 3×3, normalizare de lot, activări ReLU și conexiuni de salt pentru a păstra contextul spațial. Adâncimile filtrului progresează de obicei de la 32 la 64 la 128 la 256, echilibrând capturarea detaliilor cu costul computațional.
- Auto-Encoder Stivuit (Metoda Poster): Pipeline-ul posterului folosește în schimb un auto-encoder stivuit antrenat să reproducă intrarea ROI, învățând implicit formele camerelor ca prioritate. Gâtul său forțează rețeaua să distileze caracteristici esențiale cardiace, producând o mască inițială pixel cu pixel care alimentează etapa de refinare.
Fuziunea Modelului Deformabil pentru Buruieni Fără Flaws
Măștile de învățare profundă brute pot fi ușor zimțate sau aliniate greșit la limite complexe. Pentru a impune plauzibilitatea anatomică, conturul inițial se integrează într-un model deformabil clasic (contur activ):
- Inițializare: Ieșirea auto-encoder-ului sau U-Net oferă curba inițială.
- Minimizarea Energiei: Termenii formă și intensitate ghidează conturul pentru a urma strâns marginile camerelor reale.
- Netezirea Ieșirii: Masca finală este atât netedă cât și adecvată anatomiei precise, corectând artefactele minore de învățare profundă fără intervenție manuală.
Acest design în trei etape combină viteza și puterea de învățare a CNN-urilor cu rigurositatea geometrică a modelelor deformabile.

Antrenarea Rețelei: Rețete pentru o Segmentare Puternică
Construirea unui model care se generalizează între pacienți și scanere se bazează pe funcții de pierdere atent alese, augmentare inteligentă și protocoale de validare riguroase.
Pierderi Inteligente: Dice Se Întâlnește cu Entropia-Cross
Entropia cross pur optimizează acuratețea pixel cu pixel dar poate întâmpina dificultăți cu forța de clasă când camerele ocupă doar o fracțiune din imagine. Pierderea Dice maximizează suprapunerile dar poate fi instabilă la începutul antrenamentului. Combinarea lor produce cele mai bune rezultate.
- Entropie-Cross Ponderată: penalizează pixelii clasificati greșit, păstrând rețeaua ancorată în corectitudinea pe voxel.
- Pierdere Dice: maximizează direct suprapunerea dintre predicție și adevărul de bază, îmbunătățind astfel delimitarea marginilor.
- Regularizare L2: Îmblânzește greutățile prea mari pentru a atinge o convergență mai netedă.
Studii raportează că această pierdere hibridă depășește fiecărui component singur—îmbunătățind scorurile medii Dice pe seturi de date RMN păstrate cu 2-3 puncte procentuale.
Augmentarea Datelor pentru a Depăși Variabilitatea Scannerului
Protocolele RMN cardiac variază extrem—intensități ale câmpului, grosimi ale feliei, plane de imagistică—astfel încât augmentările simulează această diversitate.
- Transformări Geometrice: rotații (de exemplu, multipli de 60°), scalare, translații, flipuri Deformări Elastice
- Elastic Deformations: deformări netede aleatorii imită variabilitatea anatomică și mișcarea respiratorie.
- Schimbări de Intensitate: oscilațiile de contrast și luminozitate țin cont de diferențele în calibrarea scannerului.
Augmentarea în timp real garantează că modelul vede o diversitate de aproape infinite de exemple, reducând dramatic suprainvățarea și îmbunătățind performanța între furnizori.
Strategia de Optimizare & Validare
Un regim intens de antrenament garantează că înveți adevărat anatomia inimii, nu ciudățile setului de date.
- Optimizatori:Adam sau SGD cu o rată de învățare inițială ~1×10⁻⁴, redusă la jumătate la fiecare 10–20 de epoci pentru a rafina greutățile.
- Oprirea Precoce: monitorizează Dice-ul de validare; se oprește atunci când îmbunătățirea stagnează timp de 10 epoci consecutive.
- Validare-Cross: împărțiri 5-fold pe seturi de referință (ACDC, MICCAI RV/LV) pentru a evalua stabilitatea și a evita împărțirile norocoase.
Împreună, aceste alegeri stabilesc un echilibru între viteza de convergență și generalizare, oferind contururi de grad clinic în condiții din lumea reală.
Demonstrarea Performanței: Metri Ce Contează
Evaluarea segmentării RMN-ului calității se bazează pe trei metrici de bază. Fiecare surprinde un aspect distinct despre cât de aproape se potrivește masca automată cu delimitările expert.
Coeficientul de Similaritate Dice (DSC)
DSC măsoară suprapunerea volumetrică între măștile prezise și cele de adevăr de bază. Valorile variază de la 0 (fără suprapunere) la 1 (suprapunere perfectă). Modelele de vârf ating în mod obișnuit DSC > 0.90 atât pentru ventriculul stâng cât și pentru cel drept, plasând acuratețea lor pe aceeași linie cu cea a cititorilor experți.
Distanța Hausdorff (HD)
HD cuantifică cea mai gravă eroare a limitelor în milimetri, definită ca cea mai mare distanță de la orice punct de pe un contur la cel mai apropiat punct de pe celălalt. Un HD scăzut (< 10 mm) indică faptul că masca urmează în mod precis marginile anatomice subtile.
Raportarea atât a mediei cât și a deviației standard a HD ajută la dezvăluirea consistenței între scanările pacienților.
Corelația Volumului (R)
Coeficientii de corelație sunt folosiți pentru a compara măsurătorile automate și manuale ale volumului final diastolic (EDV), volumului final sistolic (ESV) și fracției de ejecție (EF). Valorile R mari (≥ 0.99) se semnalează că modelul produce metrici cuantitative echivalente clinic, asigurând încrederea în indicii funcționali ulteriori.
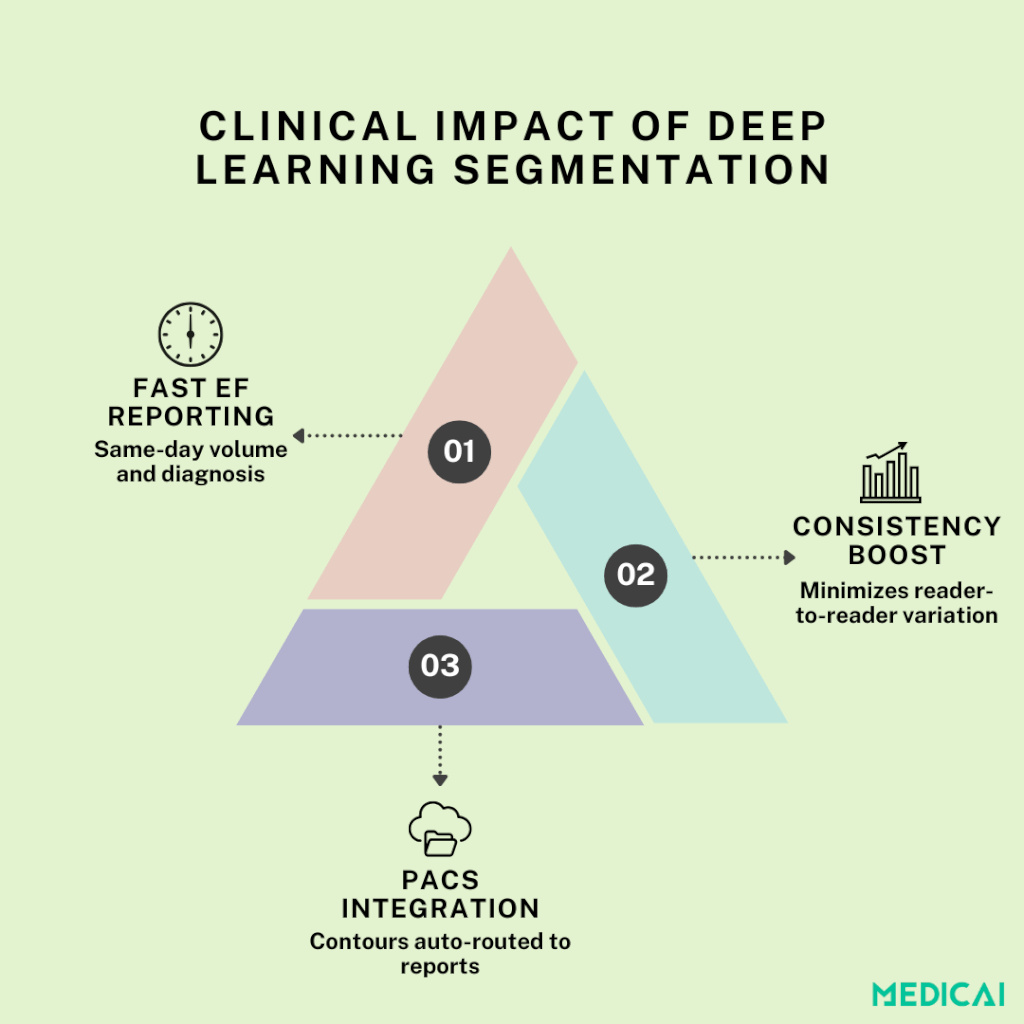
Impactul Clinic: Mai Rapid, Consistent, Scalabil
Segmentarea camerelor alimentată de învățare profundă transformă fluxurile de lucru clinice în trei moduri cheie.
Raportarea Automată a Fracției de Ejecție
Prin livrarea volumelor ventriculare precise în câteva secunde, segmentarea alimentată de AI permite calcularea în aceeași zi a volumului final diastolic (EDV), volumului final sistolic (ESV) și fracției de ejecție (EF). Aceasta revenire rapidă accelerează diagnosticul și susține ajustările de tratament în timp util, fără întârzieri în trasarea manuală.
Minimizarea Variabilității Inter-Observator
Delimitarea manuală tradițională suferă de diferențe între cititori—schimbările mici ale contururilor pot traduce în discrepanțe semnificative ale EF.
Modelele de învățare profundă ating scoruri Dice de ≥ 0.90 și corelații de volum de ≥ 0.99, asigurând măsurători constante și sporind încrederea clinicianului în monitorizarea pacienților.
Integrarea PACS/RIS fără întreruperi
Odată antrenat, pipeline-ul poate fi integrat direct în Sistemele de Arhivare și Comunicație a Imaginilor (PACS) furnizate de platforme precum Medicai sau Sistemele de Informații Radiologice (RIS).
Procesarea complet automată nu necesită interacțiune din partea utilizatorului, direcționând contururi finalizate și rapoarte cantitative în registrul medical electronic. Acestea eficientizează volumul de muncă al radiologiei.
Depășirea Obstacolelor: Limite & Soluții
În ciuda promisiunilor lor, AI în RMN pipeline-urile de segmentare trebuie să abordeze trei provocări persistente pentru a realiza o adoptare clinică pe scară largă.
Variabilitatea Scannerului
Diferențele în intensitatea câmpului, secvențele specifice furnizorilor și grosimea feliei pot degrada performanța modelului.
Soluțiile includ augmentarea extinsă a datelor pe parcursul antrenamentului (rotații, oscilații de intensitate, deformări elastice) și reglarea fină pe loturi mici de scanări noi pentru a se adapta la protocoalele locale.
Patologii Rârare (de exemplu, Hipertrofie)
Condiții neobișnuite precum hipertrofia septală asimetrică sau malformațiile congenitale pot să nu apară în seturile de antrenament standard. Acest lucru poate duce la segmentări insuficiente sau distorsiuni ale formei.
Strategiile de atenuare includ colecții de cazuri țintite, augmentare sintetică pentru anatomii extreme și utilizarea estimării incertitudinii pentru a marca ieșirile cu încredere scăzută pentru revizuire.
Ambuteiajele în Annotarea Datelor
Contururile manuale de calitate înaltă sunt intensive în muncă și costisitoare, limitând dimensiunea corpului de antrenament.
Metode precum învățarea semi-supervizată, învățarea federată și învățarea activă pot reduce necesitatea datelor etichetate prin utilizarea scanărilor neetichete, împărtășind actualizări fără a transfera date și concentrându-se pe cazuri cheie.
Concluzie
Învățarea automată automatizată permite segmentarea rapidă și precisă a camerelor cardiace în RMN cardiac, oferind contururi exacte în câteva secunde. Combină CNN pentru localizare, U-Net pentru procesare și modele deformabile pentru refinare pentru a oferi clinicianilor rezultate fiabile.
Cu integrarea turn-key PACS de la Medicai, actualizări federate ale modelului și tablouri de bord explicabile, puteți desfășura instantaneu acest pipeline de vârf. Cu noi, puteți oferi îngrijiri cardiace mai rapide și mai inteligente pentru fiecare pacient.
Articole conexe



Haideți să luăm legătura!
Aflați mai multe despre modul în care Medicai vă poate ajuta să vă consolidați practica și să îmbunătățiți experiența pacienților dumneavoastră. Sunteți gata să începeți călătoria?
Rezervați o demonstrație gratuită