KI und PACS: Revolutionierung der Radiologiepraxis

Was wäre, wenn Ihr PACS mehr könnte, als nur Bilder zu speichern? Was wäre, wenn es dabei helfen könnte, sie zu interpretieren, Fälle zu priorisieren und die Berichtserstellungszeit zu verkürzen?
Genau das bringt AI jetzt in Radiologieabteilungen auf der ganzen Welt.
Die AI-Integration in radiologischen PACS bezieht sich auf die nahtlose Einbettung von künstlichen Intelligenztools in Bildgebungsabläufe. Sie unterstützt die automatisierte Analyse, die Entscheidungsfindung in Echtzeit und intelligenteres Reporting direkt vom PACS-Viewer.
Entdecken Sie, wie es funktioniert, warum es wichtig ist und was Sie benötigen, um AI erfolgreich in Ihre PACS-Umgebung zu integrieren.

Warum die AI-Integration in PACS ein Game Changer ist
Radiologieabteilungen sehen sich heute einer wachsenden Krise gegenüber: zu viele Scans, zu wenige Hände und zunehmender Druck, schnellere und genauere Interpretationen zu liefern. Mit Burnout Raten von bis zu 62 % unter Radiologen und die Komplexität der Bilder nimmt zu, wird die Integration von AI in PACS nicht länger optional; sie ist wesentlich.
AI-Tools erhöhen die Diagnosetempo, indem sie dringende Fälle priorisieren, kritische Befunde hervorheben und Läsionen vorsortieren. Das verringert die mentale Belastung der Radiologen, sodass sie sich auf die Interpretation statt nur auf die Identifikation konzentrieren können.
Wenn diese Tools direkt in die PACS-Oberfläche integriert sind, schaffen sie nahtlose, intelligentere Arbeitsabläufe ohne zusätzliche Klicks oder Wechsel der Plattform.
Im administrativen Bereich rationalisiert AI alles, von der Terminplanung bis zur Auswahl von Protokollen und der automatisierten Berichtserstellung. Werkzeuge zur Verarbeitung natürlicher Sprache (NLP) verbessern die Diktiergeschwindigkeit und -genauigkeit, während strukturierte Berichtssysteme helfen, Konsistenz über Fälle hinweg zu gewährleisten.
Die Daten unterstreichen die Dringlichkeit. Die medizinische Bildgebung trägt jetzt etwa 90 % aller Krankenhausdaten bei, und das weltweite Volumen der radiologischen Untersuchungen wird voraussichtlich bis 2030 etwa 5 Milliarden Studien überschreiten. Ohne Automatisierung können von Menschen geführte Arbeitsabläufe einfach nicht mit dieser Nachfrage mithalten.
Verstehen der drei Reifegrade der AI-PACS-Integration
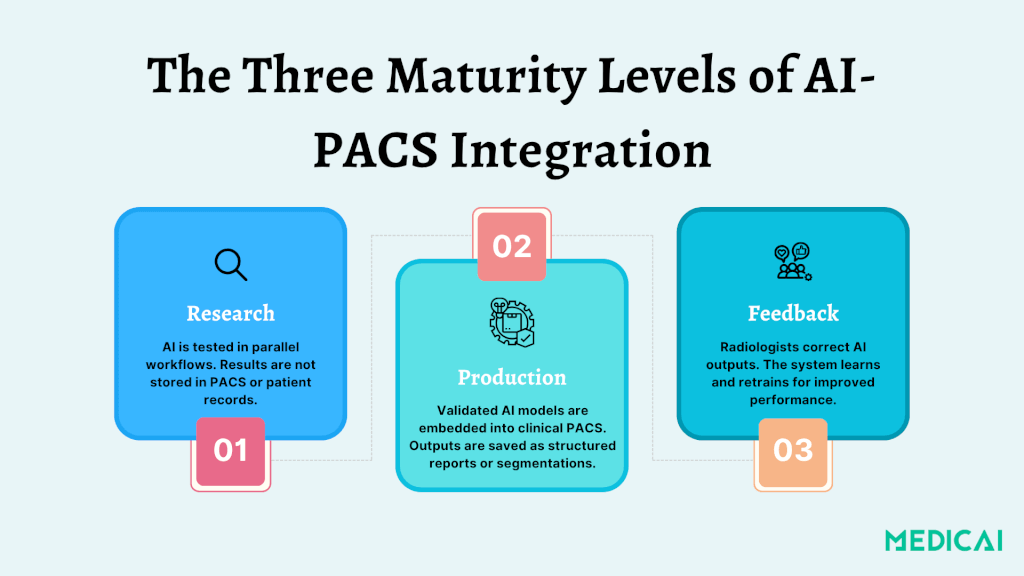
Die Integration von AI in der Radiologie umfasst drei Reifegrade in PACS, von experimentellen Overlays bis hin zu anpassbaren Systemen, die AI-Ausgaben mit der klinischen Praxis in Einklang bringen.
Stufe 1: Forschung — Testen von AI in parallelen Abläufen
In diesem Stadium werden AI-Algorithmen ausschließlich für Forschungszwecke verwendet. Radiologen können AI-generierte Segmentierungen oder Annotationen überprüfen, aber diese Ergebnisse werden nicht in die Patientenakte aufgenommen. Stattdessen gehen sie in ein separates Forschungs-PACS oder -Viewer.
Der Prozess ermöglicht es Institutionen:
- Die Modellleistung sicher ohne klinisches Risiko zu bewerten
- Abläufe vor der klinischen Bereitstellung zu optimieren
- AI-Befunde parallel mit Bewertungen von Radiologen zu vergleichen
Diese Forschungsumgebungen sind entscheidend für die regulatorische Genehmigung, Leistungsvalidierung und Sicherheitstests. Die klinische Nützlichkeit von AI ist jedoch begrenzt, da ihre Ausgaben für Kliniker nicht sichtbar sind und nicht in die Patientenakten aufgenommen werden.
Stufe 2: Produktion — AI wird Teil des klinischen Arbeitsablaufs
Sobald sie validiert sind, können AI-Modelle in klinischen PACS integriert werden. Es ermöglicht Radiologen, Befunde wie Läsionssegmentierungen und Kalziumwerte direkt innerhalb ihrer gewohnten Plattformen abzurufen und den Arbeitsablauf zu verbessern.
AI-Triage-Tools können helfen, kritische Studien zu priorisieren, automatisierte Messungen bereitzustellen und den Berichterstellungsprozess durch die Bereitstellung strukturierter Berichtssprache zu rationalisieren.
AI-Ergebnisse auf dieser Ebene werden gespeichert als:
- DICOM SEG (Segmentierungsobjekte)
- DICOM SR (strukturierte Berichte)
- GSPS (Graustufen-Softcopy-Präsentationszustände)
AI prägt aktiv diagnostische Arbeitsabläufe, beispielsweise indem sie Studien priorisiert, die auf Verdacht auf eine Lungenembolie bei CT-Triage gekennzeichnet sind. Sie beschleunigt tatsächlich die Notfallversorgung.
Stufe 3: Feedback — Kontinuierliches Lernen aus dem Input von Radiologen
Dies ist die höchste Stufe der Integration, die es Radiologen ermöglicht, AI-Ausgaben zu bearbeiten (z.B. Fehlalarme zu entfernen, Segmentierungen zu verfeinern). Es hilft, die zukünftige Leistung des Systems zu verbessern.
Eine feedbackgesteuerte Architektur umfasst typischerweise:
- Ein Zero-Footprint-Viewer zum Bearbeiten von AI-Annotationen
- Ein dedizierter Trainingsserver zum Sammeln, Validieren und Retrainieren des Modells
- Annotationenspeicherung, die die Eingaben von Radiologen sicher erfasst
Dies schafft einen kontinuierlichen Lernzyklus, der es AI ermöglicht, basierend auf klinischen Daten aus der realen Welt zu evolvieren.
In einer realen Implementierung zur Erkennung von Hirnmetastasen reduzierte das Feedbacksystem die Fehlalarme von 14,2 auf 9,12 pro Patient und erhöhte die Trainingsdatensätze von 93 auf 217 Scans. Dies führte zu einer verbesserten Leistung und einer hohen Sensitivität von 90%.
Diese Stufe verwandelt AI von einem statischen Werkzeug in einen kollaborativen Assistenten, der von Radiologen wie ein Auszubildender lernt und sich ohne vollständigen Modellumbau verbessert.
Technische Grundlagen: PACS, APIs und Workflow-Trigger
Lassen Sie uns die zentralen Komponenten aufschlüsseln, die die AI-PACS-Integration in der realen Welt funktionieren lassen.
PACS, DICOM-Standards und Bildgebungsinfrastruktur
Das Picture Archiving and Communication System (PACS) ist das Herzstück des radiologischen Workflows. Es speichert, ruft ab und zeigt medizinische Bilder an. Für eine effektive AI-Integration muss PACS standardisierte Protokolle unterstützen.
- DICOM (Digital Imaging and Communications in Medicine) für Bilder und Segmentierungen
- DICOM SR (strukturierte Berichte) für Messausgaben
- DICOM SEG (Segmentierungsobjekte) für visuelle Overlays
- GSPS (Graustufen-Softcopy-Präsentationszustände) für Bildannotations
Diese ermöglichen es, AI-generierte Ergebnisse direkt in der Umgebung des Radiologen ohne zusätzliche Plattformen oder Viewer anzuzeigen.
APIs und Interoperabilität
Die Integration beruht auf gut dokumentierten APIs und Datenstandards, um eine nahtlose Kommunikation zwischen PACS, RIS (Radiologieinformationssystem), AI-Engines und EHRs zu gewährleisten. Dazu gehören:
- HL7 für den Austausch klinischer Daten
- FHIR für moderne webbasierte Gesundheitsinteroperabilität
- RESTful APIs und DICOMweb für den Zugriff auf und die Übertragung von Bildgebungsdaten
Nicht alle PACS-Lösungen sind gleich; viele verwenden proprietäre Formate, die AI-Korrekturen behindern. Diese Fragmentierung kann zu ungeklärten AI-Fehlern führen, die Vertrauen und klinische Akzeptanz untergraben.
Orchestrierungsmaschinen und Workflow-Trigger
Eine der größten technischen Herausforderungen ist, wie und wann ein AI-Algorithmus ausgelöst wird.
Das AI-System benötigt oft manuelles Eingreifen in veralteten Arbeitsabläufen, wie das Routing spezifischer Bildserien vom PACS zum AI-Server. Dieser Prozess ist fehleranfällig; das Senden der falschen Serie oder ein fehlerhafter Trigger kann zu ungültigen oder unvollständigen AI-Ausgaben führen.
Um dies zu lösen, nutzen moderne Systeme eine AI-Orchestrierungsmaschine, die automatisiert:
- Bilder von Modalitäten (CT, MRT) zum AI-Server leitet
- Daten in Echtzeit verarbeitet (Edge- oder cloudbasiert)
- Ausgaben direkt an den PACS-Viewer zurückgibt
- AI-Ausführungen zur Nachverfolgbarkeit protokolliert
Orchestrierungsmaschinen ermöglichen auch Mehrserien-Eingaben, die für komplexe Aufgaben wie zeitliche Vergleiche, 3D-Segmentierung oder langfristige Krankheitsüberwachung notwendig sind.
Cloud vs Edge Computing
Je nach Anwendungsfall und Infrastruktur kann die AI-Inferenz erfolgen:
- In der Cloud (skalierbar, ideal für Training oder Multi-Site-Zugriff)
- Am Edge (schneller, ideal für Echtzeit-Triage oder intra-prozedurale AI)
Eine Studie hat gezeigt, dass Cloud-Lösungen Flexibilität und Skalierbarkeit bieten, während Edge-Geräte die Latenz reduzieren und eine Bearbeitungszeit von unter einer Sekunde bei zeitkritischer Bildgebung wie Ultraschall oder Trauma ermöglichen.
Daher müssen Krankenhäuser sorgfältig bewerten:
- Netzwerkbandbreite
- Verfügbarkeit von GPU-Hardware
- Datenschutz und HIPAA-Compliance
- Kapazität des IT-Teams zur Verwaltung von Updates, Sicherheit und Speicherung
Workflow der AI-Integration in radiologischen PACS
Entdecken Sie, wie AI typischerweise in den radiologischen Workflow integriert wird, sobald sie in PACS integriert ist.
Schritt 1: Bildakquisition und Routing
Der Workflow beginnt, wenn eine Modalität (CT, MRT, Röntgen) eine Bildstudie aufnimmt. Die resultierenden DICOM-Dateien werden dann automatisch über den DICOM-Router geleitet, ein System, das Bilder weiterleiten kann an:
- PACS (für Archivierung und klinische Überprüfung)
- Anbieterneutrale Archive (VNA)
- AI-Engines (für Verarbeitung und Analyse)
In einem AI-integrierten Workflow werden Bilder automatisch oder selektiv an ein AI-System basierend auf vordefinierten Regeln wie Modalitätstyp, Körperteil oder Protokoll gesendet.
Schritt 2: AI-Verarbeitung und Inferenzgenerierung
Sobald empfangen, verarbeitet die AI-Engine die Bilder, um eine spezifische Aufgabe auszuführen, wie zum Beispiel:
- Läsionserkennung (Lungenknoten, Hirnmetastasen)
- Organsegmentierung (Leber, Herzkammern)
- Klassifizierung von Anomalien (Frakturen, Ergüsse)
- Risikobewertung oder Triage (PE, Schlaganfall)
Die AI generiert Ergebnisse in standardisierten Formaten wie:
- DICOM SEG (Segmentierungsmaske)
- DICOM SR (strukturierte Berichte mit Messungen)
- GSPS (Graustufen-Overlays)
Diese Ausgaben sind mit Versionskennungen und relevanten Metadaten versehen, die Nachverfolgbarkeit und Auditbereitschaft gewährleisten.
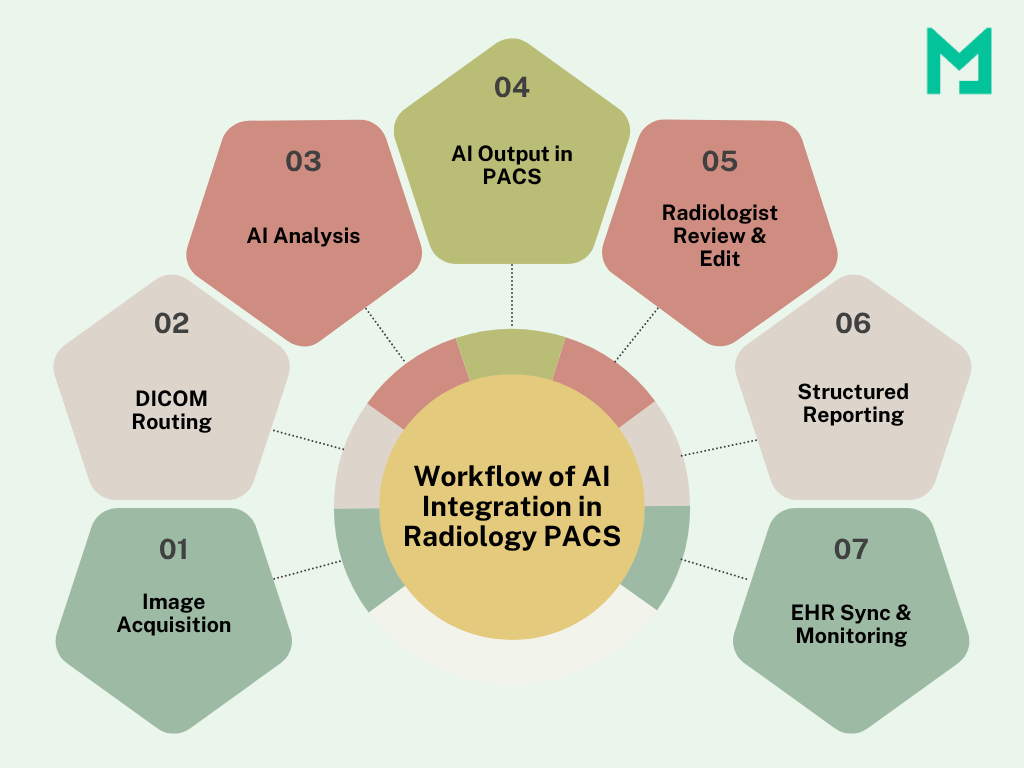
Schritt 3: Ergebnisbereitstellung im PACS-Viewer
Die AI-Integration in radiologischen PACS zielt darauf ab, Einblicke innerhalb der Lesesituation des Radiologen zu bieten. AI-Ausgaben erscheinen als neue Serien oder Overlays im PACS-Viewer, was einen einfachen Vergleich mit den Originalbildern ermöglicht.
Einige Workflows können Arbeitslisten priorisieren, indem sie dringende Fälle basierend auf AI-Befunden kennzeichnen.
Im Gegensatz zu eigenständigen AI-Dashboards stellt die PACS-Integration sicher, dass AI-Einblicke kontextuell bereitgestellt werden, ohne zusätzliche Klicks oder Plattformwechsel.
Schritt 4: Überprüfung, Feedback und Berichterstattung durch den Radiologen
Radiologen überprüfen sowohl die Rohbilder als auch die AI-verbesserten Ausgaben. Organisationen reagieren auf AI-Befunde, indem sie sie akzeptieren, modifizieren oder Feedback geben. Feedbackschleifen helfen, die AI im Laufe der Zeit zu verbessern.
Schritt 5: Berichtserstellung und EHR-Integration
Endgültige radiologische Berichte können von AI abgeleitete Messungen oder Befunde enthalten, insbesondere in strukturierten Berichtsumgebungen. Diese sind:
- Automatisch im RIS oder Berichtssystem vorausgefüllt
- Mit der elektronischen Patientenakte (EHR) für den Zugriff der Klinikern synchronisiert
- Neben Bilddaten in PACS zu medico-rechtlichen Zwecken
Schritt 6: Überwachung und Governance
Nach dem Start des Workflows ist die Überwachung der Systemverfügbarkeit und der AI-Latenz wichtig für die Effizienz. Die Bewertung der Ausgabe-Genauigkeit und der Nutzungsmuster sowie das Verfolgen des Feedbackvolumens und der Modellabweichung sind entscheidend für die Aufrechterhaltung der Zuverlässigkeit.
Die Vorteile: Warum AI in PACS den Hype wert ist
Lassen Sie uns prüfen, wie AI PACS zugutekommt.
Schnellere Reaktionszeiten und Priorisierungen
AI hilft Radiologen, kritische Fälle in Umgebungen mit hohem Volumen zu priorisieren, indem sie Scans für Zustände wie intrakraniellen Blutungen oder Lungenembolien schnell kennzeichnet. Dadurch wird die Triage von lebensbedrohlichen Situationen beschleunigt, was Verzögerungen bei Diagnosen reduziert.
Eine Studie berichtete von einer 24 %igen Reduktion der durchschnittlichen Berichtszeit als Radiologen AI-unterstützte Werkzeuge zur Interpretation verwendeten.
Verbesserte Qualitätskontrolle und Fehlerreduktion
AI ermüdet nicht und ist ein zweiter Leser, der das diagnostische Vertrauen steigert, indem er übersehene Befunde identifiziert. In klinischen QA-Systemen reduzierte es den Prüfaufwand für Radiologen um 98,5 %, indem subtile Probleme aufgedeckt wurden, die möglicherweise unbemerkt geblieben sind.
Verbesserte Skalierbarkeit
Radiologieabteilungen werden voraussichtlich immer größer werdende Bildvolumina zu bewältigen, ohne dass sich das Personal proportional erhöht. AI hilft, dieser Nachfrage nachzukommen, indem sie sich wiederholende Aufgaben übernimmt und beim frühzeitigen Verständnis unterstützt.
Kontinuierliches Lernen und Feedbackschleifen
In fortgeschritteneren Implementierungen können Radiologen AI-Ausgaben bearbeiten oder korrigieren, die in das Modell zurückgeführt werden, um wieder zu trainieren und die Leistung zu verbessern. Dies ist besonders wertvoll in dynamischen Bereichen wie der Neurobildgebung, Onkologie und Traumatologie.
Die Herausforderungen: Was die Integration zurückhält
Die Integration von AI in PACS hat Potenzial, sieht sich jedoch oft Hindernissen gegenüber.
Workflow-Fragmentierung
Eine große Beschwerde von Radiologen ist, dass AI-Tools isoliert arbeiten, separate Anmeldungen erfordern und den Workflow stören. Das verringert die Wahrscheinlichkeit, AI-Einblicke zu verwenden.
Stellen Sie sicher, dass AI-Ausgaben direkt in PACS-Viewer als DICOM SEG oder SR-Objekte eingebettet sind.
Begrenzte Korrekturmöglichkeiten
Viele kommerzielle PACS-Systeme erlauben es Radiologen nicht, AI-generierte Ausgaben zu bearbeiten oder zu korrigieren. Das schränkt die Möglichkeit des Modells ein, sich zu verbessern, und discouragiert die Nutzerbeteiligung.
Übernehmen Sie PACS-Systeme oder AI-Interfaces, die Feedback und editierbare Overlays unterstützen, um kontinuierliches Lernen zu ermöglichen.
AI-Auslösungen und Routingfehler
Das manuelle Routing von Bildern zur AI-Engine kann fehleranfällig sein, insbesondere bei komplexen Studien mit mehreren Serien. Die AI kann irrelevante Daten verarbeiten oder das beabsichtigte Ziel verfehlen, wenn die falsche Serie geroutet wird.
Verwenden Sie Orchestrierungsmaschinen, die die Serienauswahl automatisieren, Metadaten validieren und Bilder basierend auf vordefinierter Logik routen.
Regulatorische Komplexität
Die Bereitstellung von AI in klinischen Umgebungen erfordert die Einhaltung von Sicherheits- und Datenschutzrichtlinien, wie FDA-Zulassung und HIPAA. Schlechte Planung kann die Implementierung verlangsamen.
Entwickeln oder übernehmen Sie ein Qualitätsmanagementsystem (QMS), das mit diesen Standards in Einklang steht, um die Bereitstellung zu optimieren und die zukünftigen Prüfungen zu erleichtern.
Infrastruktur- und Kostenbelastungen
Die AI-Verarbeitung großer Datensätze wie 3D-MRIs oder Multi-Phase-CTs erfordert erhebliches Rechenpotential und Speicherplatz. Cloud-basierte AI könnte Latenz- oder Sicherheitsprobleme erhöhen, während örtliche Edge-Geräte neue Hardware und Energiemanagement benötigen könnten.
In Betracht ziehen Sie ein hybrides Cloud-Edge-Modell unter Verwendung von lokalen GPU-Servern für dringende Verarbeitung und der Cloud für großangelegtes Training oder Archivierung.
Fazit
Die AI-Integration in radiologischen PACS verändert heute die klinischen Arbeitsabläufe. Wenn AI-Einblicke nahtlos innerhalb des PACS bereitgestellt werden, gewinnen Radiologen Geschwindigkeit, Genauigkeit und Unterstützung ohne zusätzliche Komplexität.
Da kommt Medicai ins Spiel—und hilft Gesundheitssystemen, die Lücke zwischen Innovation und Benutzerfreundlichkeit zu schließen.
Warum warten? Modernisieren Sie Ihren Bildgebungsworkflow.
Verwandte Artikel



Das Gespräch beginnen
Erfahren Sie mehr darüber, wie Medicai Ihnen helfen kann, Ihre Praxis zu stärken und die Patientenerfahrung zu verbessern. Sind Sie bereit, Ihre Reise zu beginnen?
Kostenlose Demo buchen